
一、临床、影像、病理和相关术语
摘要
纤维化间质性肺疾病中肺气肿较为常见,两者合并存在被称作肺纤维化合并肺气肿(CPFE)综合征。由于目前国际上缺乏CPFE统一的定义和诊断标准,2022年美国胸科学会(ATS)/欧洲呼吸学会(ERS)/日本呼吸病学会(JRS)/拉丁美洲胸科联盟(ALAT)发表的研究共识对CPFE进行了详细描述。本文旨在对该研究共识中CPFE的临床表现、影像学与病理学特征和相关术语等内容进行解读,以便进一步提高对CPFE的临床认识和诊治水平。
【关键词】肺纤维化;肺气肿;研究共识;解读
肺气肿在包括特发性肺纤维化(idiopathic pulmonary fibrosis,IPF)在内的纤维化间质性肺疾病(fibrotic interstitial lung disease,f-ILD)患者中较为常见,被命名为“肺纤维化合并肺气肿(combined pulmonary fibrosis and emphysema,CPFE)综合征”[1-2]。影像学上CPFE除见于IPF合并肺气肿,还表现为气腔扩大伴纤维化(airspace enlargement with fibrosis,AEF)[3]和吸烟相关性肺间质纤维化(smoking-related interstitial fibrosis,SRIF)[4]等。2022年9月,由ATS/ERS/日本呼吸病学会(Japanese Respiratory Society,JRS)/拉丁美洲胸科联盟(Asociacion Latinoamericana de Torax,ALAT)的代表组成的委员会对CPFE的定义和特征等进行描述,确定其是否代表一种综合征、处理方法和研究重点。本文将重点解读研究共识中CPFE流行病学、病因学、临床表现、影像学与病理学特征、相关术语、CPFE的研究定义与CPFE临床综合征的分类标准等内容。
1、CPFE的研究历程和流行病学
CPFE的概念最早是在1948年提出的,随后发现CPFE患者的肺容积基本正常或轻度下降,但肺弥散功能严重降低[5],组织病理学表现为肺气肿、炎症和纤维化改变[6],CPFE还可以表现为SRIF、呼吸性细支气管炎相关ILD和AEF等[7]。2009年,Cottin和Cordier[2]两位学者建议将CPFE作为一种综合征。
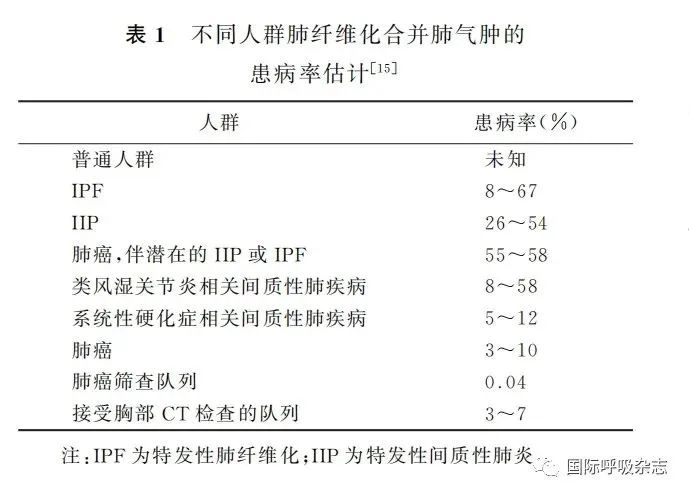
据报道,在不同人群中CPFE的流行病学不同。目前,CPFE在普通人群中缺乏患病率数据,在IPF患者中的估计患病率为8%~67%[8-10];在特发性间质性肺炎(idiopathic interstitial pneumonia,IIP)患者中患病率约26%~54%[11-12];肺癌患者中也有较高的患病率[13];在接受胸部高分辨率CT(high resolution CT,HRCT)检查的男性群体中患病率约7.3%[14](表1)。根据地域差异,亚洲和希腊CPFE的患病率最高,美国最低。
2、病因学
2.1 暴露与疾病
研究发现男性和吸烟与CPFE密切相关,男性患者CPFE的发生率增加9倍[16]。几乎所有CPFE患者均有吸烟史,平均吸烟史为40包年,并且CPFE患病与吸烟量之间存在剂量效应关系,肺气肿通常先于f-ILD出现[1]。
在非吸烟者中,结缔组织病(connective tissue disease,CTD)是CPFE的危险因素[10,17-18]。约5%~10%的系统性硬化症相关ILD患者可出现CPFE的影像学表现[19-21]。不吸烟的类风湿关节炎(rheumatoid arthritis,RA)相关ILD患者中,有27%胸部HRCT显示肺气肿存在[18]。另有研究报道在RA-ILD群体中,肺气肿发生率高达48%[10,22]。CPFE在系统性血管炎患者中也有报道,特别是显微镜下多血管炎[23-24]。胸部影像学上CTD相关普通型间质性肺炎(usual interstitial pneumonia,UIP)患者的肺气肿范围小于IPF患者[25]。
多种职业性和吸入性暴露与CPFE有关[26-28]。CPFE可见于石棉肺、矽肺和纤维化性过敏性肺炎患者[29-30]。长期暴露于蒸汽、灰尘、气体和烟雾等职业环境与影像学上更广泛的肺气肿相关[31](表2)。

2.2 遗传易感性与衰老
遗传易感性结合吸烟或暴露于空气污染物等危险因素,可能更易形成CPFE[2]。据报道,较短的端粒与COPD和IPF均相关[32]。表观遗传的改变也可能与CPFE有关[33](表2)。
3、CPFE发病机制
目前,导致肺气肿与肺纤维化共存的发病机制尚不清楚。但研究发现,肺纤维化和肺气肿有聚集性(即各种f-ILD患者发生肺气肿的风险增加),支持两者存在共同病理生理学机制[34]。肺气肿和肺纤维化之间有机械力双向作用[35],也存在多个共同通路和发病机制,包括基因表达和通路、基因突变、端粒功能障碍和缩短、肺泡的改变、表观基因组重编程和酶(特别是基质金属蛋白酶)的活性。在一些动物模型中,肺气肿和肺纤维化同时出现[6,36-37],然而,在肺气肿和肺纤维化之间也存在不同的基因突变和通路[33]。
4、临床表现和合并症
CPFE患者的平均年龄范围为65~70岁[1,16](与IPF和COPD相当),男性占73%~100%[1,38]。主要症状包括劳力性呼吸困难和咳嗽[1,14]。合并肺动脉高压者活动后呼吸困难明显,多数患者心功能分级为NYHA Ⅲ或Ⅳ级[39]。
CPFE患者常见的两种合并症为肺癌和肺动脉高压,其他合并症包括冠状动脉疾病、周围血管疾病和糖尿病[40-41]。
5、肺功能
CPFE患者运动耐力受限,DLCO和转移系数(transfer coefficient,KCO)明显降低[1,16],气体流速和肺容积相对正常,大多数患者FVC/DLCO比值增加[17]。与单独IPF相比,CPFE患者肺容积(FVC和肺总量)较高,第1秒用力呼气容积(forced expiratory volume in one second,FEV1)大致相当,残气量较高,DLCO、KCO、PaO2较低[42](表3)。

目前没有监测CPFE疾病进展的最佳肺功能指标,虽然FVC是判断IPF病情进展的重要因素,但判断CPFE疾病进展应该结合临床、影像学和多个肺功能参数,而不是强调FVC的变化趋势。
6、影像学特征
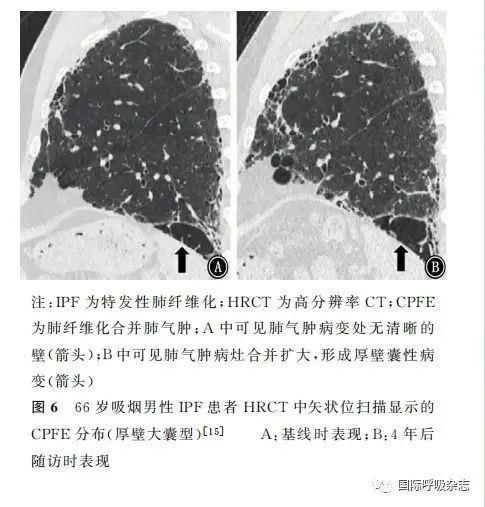
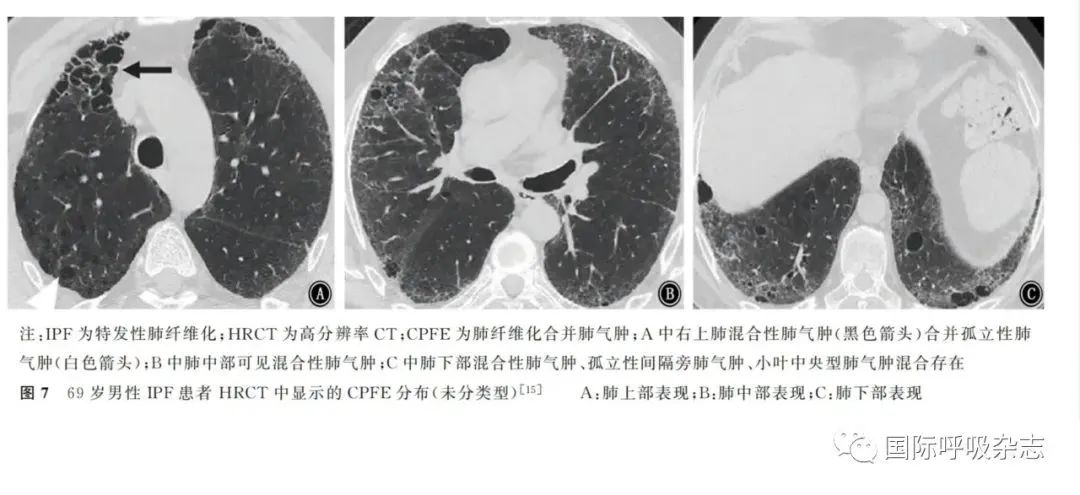
CPFE的胸部HRCT影像学特征是肺气肿和间质纤维化并存,表现多样。肺气肿被定义为低密度区域,无可见的壁[43],分为小叶中央型、间隔旁型、全小叶型[44]。间质纤维化被定义为实质衰减增加的区域,表现为网格影和(或)磨玻璃影,与蜂窝影和(或)牵拉性支气管扩张有不同程度的相关性。CPFE患者的HRCT表现中,肺气肿可初步划分为不同类型:独立的肺气肿和纤维化型、进行性转变型、间隔旁肺气肿型、混合型、厚壁大囊型和未分类型[45](图1~7)。由于CPFE患者影像学UIP型更多见,所以影像学上区分混合性肺气肿和蜂窝影具有一定挑战性。肺气肿和肺纤维化共存时可以形成厚壁囊状影,随着时间推移,肺气肿可能由于邻近肺纤维化的收缩被牵拉扩张,形成牵拉性肺气肿。
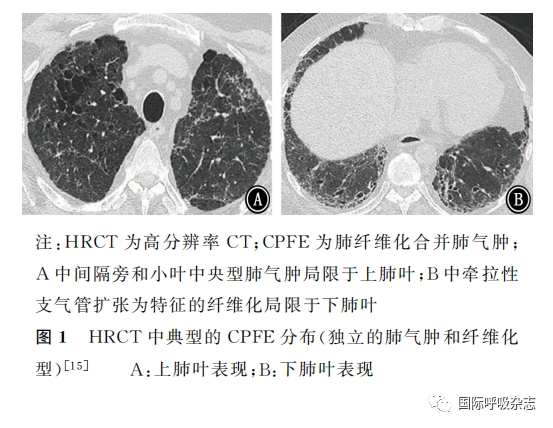
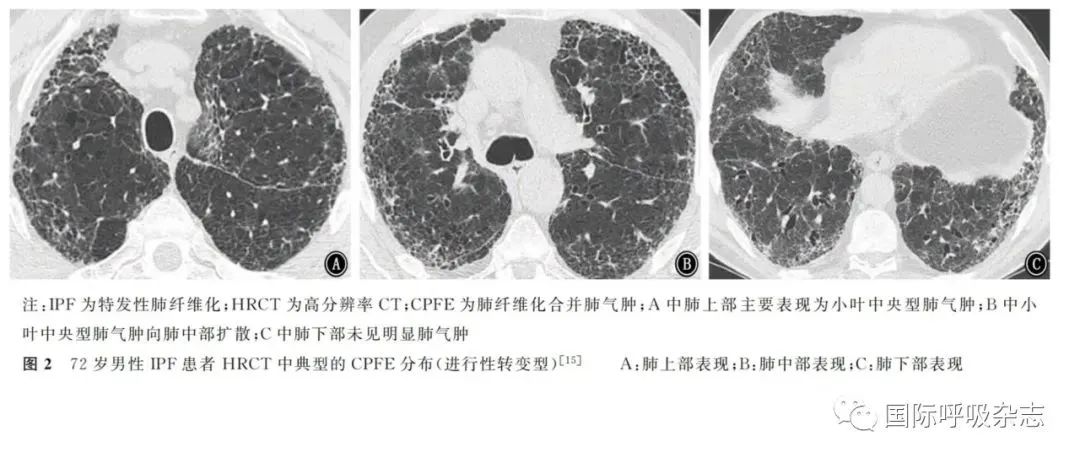
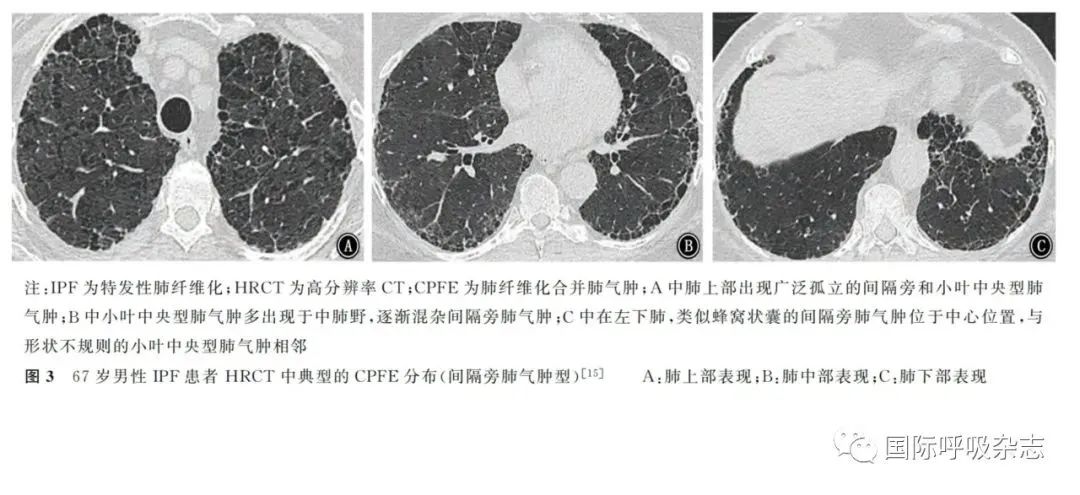
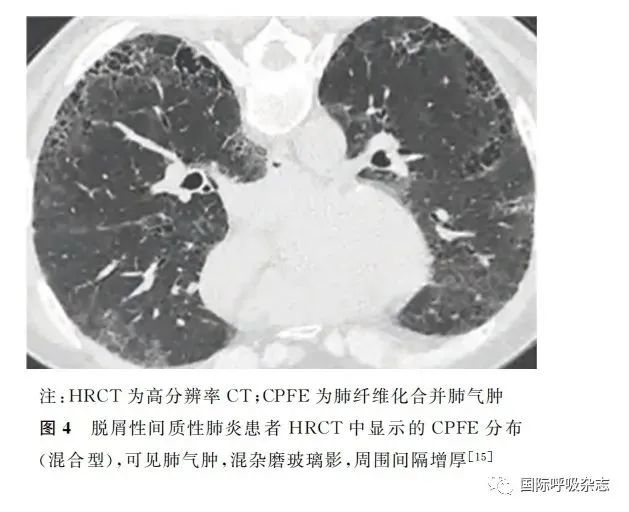

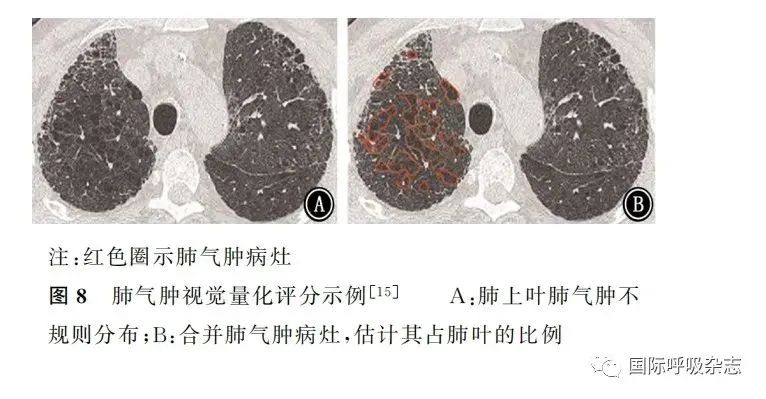
评估肺气肿程度应选择在隆突水平,先采用视觉模糊评分定量评估,累加评分后确定肺气肿程度,包括:>0%、>5%、>10%和>15%的总肺容积。建议根据肺气肿占比≥5%的总肺容积定义CPFE(图8)。
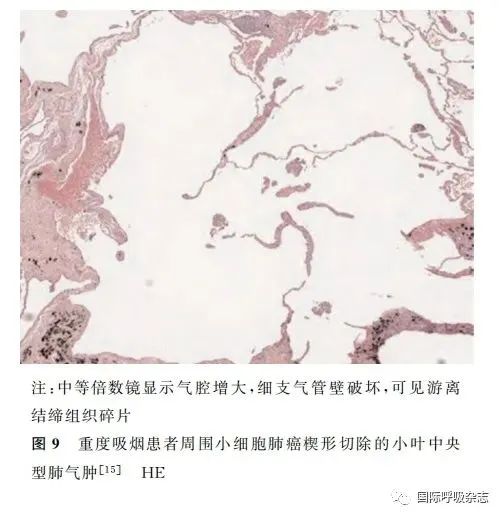
7、病理学特征
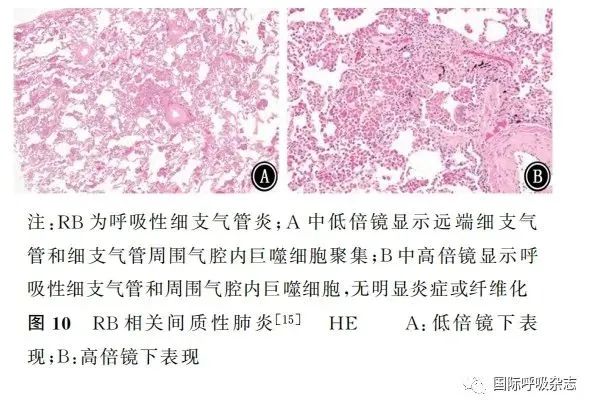
肺气肿是诊断CPFE的必要条件,被定义为异常的、永久性的细支气管远端气腔增大,伴有气道壁破坏,无明显纤维化[46](图9)。除肺气肿外,吸烟相关病理学异常包括呼吸性细支气管炎(respiratory bronchiolitis,RB)和SRIF[4,47],RB几乎只发生于吸烟者,特征为呼吸性细支气管和细支气管周围气腔内肺泡巨噬细胞聚集,无明显炎症或纤维化[45](图10),可能与其他类型的肺纤维化伴随出现,特别是SRIF、脱屑性间质性肺炎(desquamative interstitial pneumonia,DIP)、UIP和朗格汉斯细胞组织细胞增多症。与吸烟相关的独特形式的纤维化被定义为SRIF[3,7],其组织病理学特征为扩张的肺泡间隔中沉积密集的嗜酸性胶原,肺结构完整,很少或没有炎症改变(图11)。

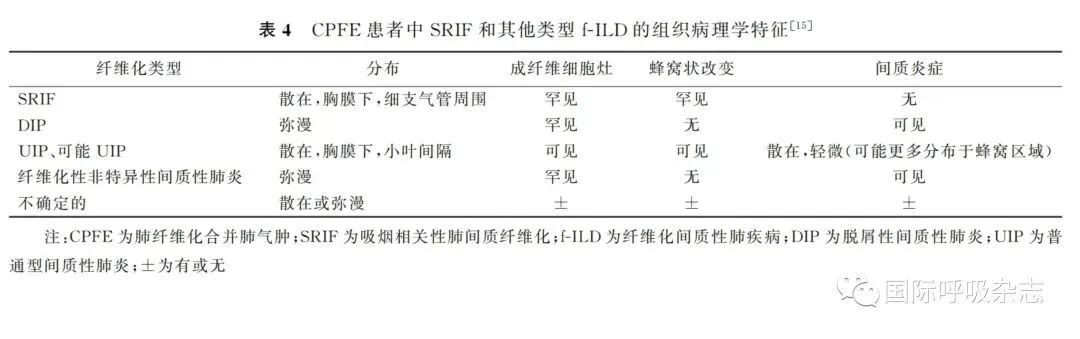
CPFE患者观察到的纤维化在组织病理学上并不对等[48](表4)。SRIF更倾向于周围胸膜下和细支气管周围分布,当合并间隔旁肺气肿时,SRIF可表现为“厚壁囊性病变”,这不同于UIP的蜂窝影,是CPFE的特征性表现[49](图12)。

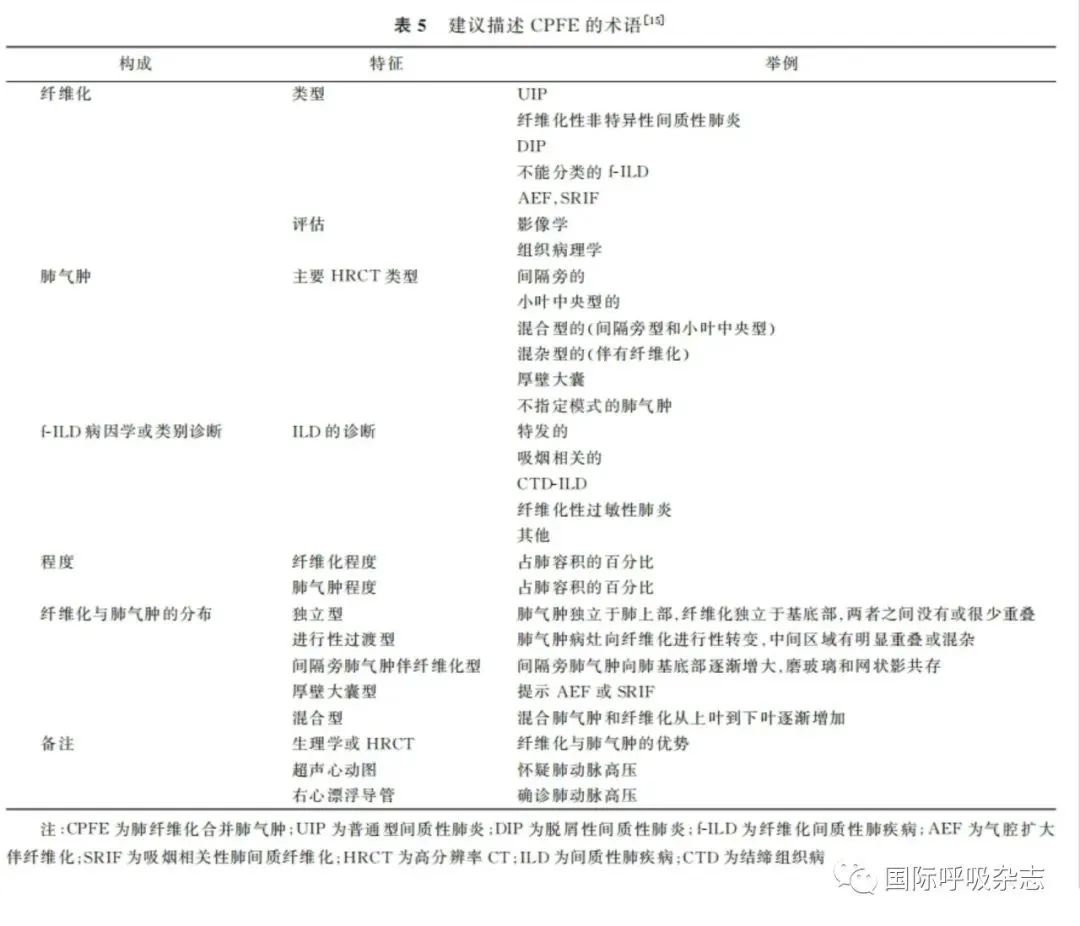
8、建议的CPFE的术语
由于缺乏对CPFE的诊断标准,所以无法进行人群间的比较,影响了生物学、临床治疗和预后的研究推进。因此有必要建立特定的CPFE标准,包括同时量化肺气肿和肺纤维化的标准的、可重复的方法。该研究共识提出描述CPFE的共同术语,见表5。
9、建议的CPFE定义
该研究共识根据近年来的文献报道,对研究中使用的CPFE定义和诊断标准进行总结,见表6。同时,该共识还提出了CPFE临时的、广泛应用的研究定义,以及CPFE临床综合征的临时分类标准。CPFE的研究定义为(1)肺纤维化和肺气肿并存;(2)患者必须同时具备HRCT的两个标准:①HRCT上,任何亚型的肺气肿定义为界限清晰的低密度区域,有极薄的壁(<1 mm)或无壁,至少累及肺总容积的5%;②肺纤维化的任何亚型。CPFE临床综合征的分类标准为患者必须符合CPFE的研究定义和以下一项或多项:(1)肺气肿程度≥肺总容积的15%;(2)相对保存肺容积和气流,伴有DLCO显著或不成比例降低,特别是HRCT异常程度有限且无肺动脉高压的患者;(3)毛细血管前肺动脉高压被认为与单纯的肺气肿(FEV1>60%)、纤维化(FVC>70%)或病因(如没有CTD)无关。

10、总结
CPFE的特征表现为肺纤维化和肺气肿共同存在,胸部HRCT和组织病理学上有多种表现和类型。肺纤维化和肺气肿的聚集(无论哪种类型的f-ILD)、相关合并症和并发症(特别是肺动脉高压和肺癌)的发生率、疾病进展监测的相关性,以及肺纤维化和肺气肿共同的疾病通路均提示CPFE应该被视为一种综合征。ATS/ERS/JRS/ALAT研究共识提供了CPFE的研究定义和CPFE临床综合征的分类标准,有利于更好地描述该疾病,了解其发病机制,指导疾病管理。
(参考文献略)
基金项目:国家自然科学基金(82070064)
作者:刘梦影 曹孟淑 - 南京大学医学院附属鼓楼医院呼吸与危重症医学科,南京 210008;通信作者:曹孟淑,Email:mengshucao@nju.edu.cn
引用本文:刘梦影,曹孟淑.《肺纤维化合并肺气肿综合征ATS/ERS/JRS/ALAT研究共识》解读(一):临床、影像、病理和相关术语[J].国际呼吸杂志,2023,43(11):1258-1266.DOI: 10.3760/cma.j.cn131368-20231016-00255.
二、定义、综合管理及未来研究重点
摘要
以往的研究将患者肺部同时存在肺气肿与肺纤维化称为“肺纤维化合并肺气肿(CPFE)”,尽管已有多项关于CPFE的研究,但人们对其定义和管理的了解仍较少。2022年美国胸科学会/欧洲呼吸学会/日本呼吸病学会/拉丁美洲胸科联盟发表的研究共识阐述了CPFE的定义、特征、病理生理机制、综合管理和研究重点等,并建议将CPFE明确为一种综合征,提出了CPFE的研究定义和分类标准,同时建议CPFE的研究应包括对影像学和病理学的全面描述。本文就该研究共识中关于CPFE综合征的定义、患者的综合管理及未来研究重点的部分进行解读。
【关键词】肺纤维化;肺气肿;综合征;管理;临床研究
早在2005年,已有研究者提出肺纤维化合并肺气肿(combined pulmonary fibrosis and emphysema,CPFE)[1]。他们在研究中观察到部分患者肺部同时存在肺纤维化和肺气肿,这类患者与单纯的纤维化间质性肺疾病(fibrotic interstitial lung disease,f-ILD)患者不同,FVC、肺总量等反映容积改变的肺功能参数减低并不显著,反映弥散功能的DLCO却明显降低,患者多存在较为严重的氧合功能障碍。尽管肺气肿和肺纤维化共存的现象得到了广泛的认可,但是一直以来缺乏统一的诊断标准,这阻碍了对CPFE生理学、综合管理和预后评估的研究。在这种背景下,有必要建立CPFE的具体标准,包括明确可重复的、标准的对肺气肿和纤维化进行定量的方法。2022年ATS/ERS/日本呼吸病学会(Japanese Respiratory Society,JRS)/拉丁美洲胸科联盟(Asociacion Latinoamericana de Torax,ALAT)发表的研究共识中正式提出CPFE是一种综合征,不同病因导致的纤维化合并肺气肿均归为CPFE的范畴,并且对CPFE的临床和研究判断标准作出明确界定。本文就该研究共识中CPFE综合征的定义、患者的综合管理、临床试验和研究前景等内容进行解读。
1、CPFE是一种综合征
根据Scadding[2]的定义,症状和体征具有明显相似表征的患者可能患有同类疾病,这种可识别的表征被称为“综合征”,具体来说强调了综合征的识别和关联性,相似的特征可用来辅助识别这类患者的特点,同时这种相似性可以帮助临床医师对疾病进行诊断、治疗和预后评估,并为进一步研究提供帮助。
CPFE被定义为一种综合征,一方面是因为纤维化和肺气肿的共存是这一组疾病的共同特征,监测疾病进展不能完全依靠FVC,FVC的变化通常用来评估特发性肺纤维化(idiopathic pulmonary fibrosis,IPF)对患者肺功能的影响,但在合并肺气肿的IPF患者中,FVC对于评估预后的贡献不如没有合并肺气肿的IPF患者;另一方面,从合并症的角度来看,肺癌和肺动脉高压(pulmonary hypertention,PH)的高患病率[3-5]更能支持将CPFE定义为一种综合征[6],而且CPFE的临床预后与单纯纤维化不同,也支持将其列为一种综合征。但是,由于在CPFE中肺气肿和f-ILD组成的异质性,以及对其量化的困难在很大程度上阻碍了对CPFE预后的评估,仍需要在统一标准诊断后,进行更多设计严谨的临床研究,为进一步全面了解CPFE提供依据。
2、CPFE患者的综合管理
2.1 一般措施
目前缺乏足够数据,也无临床实践指南指导CPFE患者的治疗。有研究提倡CPFE需要基于个体化制定治疗方案[7-8],但暂无高质量的数据能说明在CPFE的背景下治疗肺气肿或PH可以改善这些患者的疾病结局。表1中总结的CPFE管理方法是从单纯COPD患者和CPFE-IPF亚型患者的试验数据中推演得出的。

戒烟适用于所有持续吸烟的患者,同时需要避免其他潜在的吸入性暴露。辅助氧疗通常用于静息状态下的低氧血症患者,静息正常而在运动期间和夜间发生的低氧血症患者也可能获益[10]。多数CPFE患者需要定期的运动和呼吸康复治疗,虽然没有研究评估CPFE患者的呼吸康复情况,但呼吸康复和定期运动仍是肺气肿患者管理的基石,并越来越多地用于f-ILD患者。多数COPD和f-ILD的加重与呼吸道感染(病毒、细菌)有关,因此,除非有禁忌,患者需要按时接种流感、肺炎球菌和新型冠状病毒疫苗[11]。对于进展的CPFE[12],特别是在合并PH时[13],患者应尽早考虑肺移植。
2.2 肺纤维化的治疗
关于肺纤维化药物的治疗决策是以f-ILD的基础诊断为指导的。CPFE患者肺纤维化的治疗经验主要来自尼达尼布和吡非尼酮的临床试验,这两种抗纤维化药物可延缓轻、中度IPF患者FVC降低的速度。虽然合并显著肺气肿[肺气肿体积大于高分辨率CT(high resolution CT,HRCT)上纤维化体积]和有严重气流阻塞的患者常被排除在临床研究之外,但是INPULSIS试验的亚组分析仍然显示,尼达尼布治疗合并肺气肿的IPF患者延缓FVC下降的效果与不合并肺气肿患者比较差异无统计学意义[14]。在除IPF以外的其他进展性纤维化性ILD患者的临床试验中(INBUILD研究)发现,尽管给予尼达尼布治疗但疾病仍在进展[15],且不同ILD患者的治疗效果一致[16]。因此,抗纤维化药物治疗可能对CPFE的IPF亚型有效,但在CPFE的其他肺纤维化表型中并不能阻止疾病进展。对于除IPF外的f-ILD患者合并肺气肿,包括纤维化型过敏性肺炎(fibrotic hypersensitivity pneumonitis,fHP)和结缔组织病相关的ILD,糖皮质激素和(或)免疫抑制治疗可能是有益的[11]。但是,考虑到CPFE独特的生理学特性,有必要在未来的试验中加以专门的研究,具体来说,比如CPFE患者的FVC不变和以较慢的速率下降表明,如果按照IPF试验的传统将FVC作为CPFE的主要终点,则可能存在严重缺陷。
2.3 肺气肿的治疗
考虑到缺乏针对CPFE治疗的研究数据,建议区分每个患者的个体表型[17]。吸入支气管扩张剂可能对有显著气流阻塞(即COPD)的CPFE患者有利[18],另外一项无对照的队列研究表明使用吸入性糖皮质激素和长效支气管扩张剂可能改善第1秒用力呼气容积(forced expiratory volume in one second,FEV1)[10]。由于CPFE患者的肺活量数值相对良好,需要对是否联合吸入性糖皮质激素的支气管扩张剂进行进一步研究。
虽然手术或支气管镜肺减容治疗可以去除肺气肿组织,使相对正常的肺组织复张,但是,由于患者DLCO常严重降低[19],大多数CPFE患者被排除在手术适应证之外。尽管没有与手术进行直接比较,但通过支气管镜进行的支气管内瓣膜置入通常更安全[20]。目前尚不能确定切除肺气肿组织是否会导致CPFE患者的肺功能改善或者恶化。
2.4 PH的治疗
存在CPFE的情况下,PH的管理重点在于平衡潜在的呼吸系统稳态失衡,例如可以通过氧疗纠正低氧血症,协助明确肺移植的最佳时机。有研究数据不支持使用口服药物治疗PH[21-22],包括内皮素受体拮抗剂(波生坦、安贝生坦)、5型磷酸二酯酶抑制剂(西地那非、他达拉非)和可溶性鸟苷酸环化酶刺激剂(利奥西呱)[23],但有非对照的观察性研究表明上述药物治疗PH可能有益[24-25],也有研究鼓励在IPF的治疗中使用西地那非[26-28],需要特别谨慎的是,安贝生坦和利奥西呱可能对f-ILD患者并无益处[29-30],特别是CPFE患者[31]。最近的研究表明,与安慰剂相比,在ILD患者和经右心导管检查明确的第3类毛细血管前PH患者中,雾化曲前列环素可改善6分钟步行距离,降低N端前脑利钠肽浓度,改善FVC,降低临床恶化的风险[6,32]。由于存在多重挑战,临床实施仍然有限制。迄今为止,回顾性数据尚未显示PH治疗对CPFE患者的生存有益处,仍需要进一步的研究具体评估这些治疗,特别是对那些肺活量和PH病情不成比例的患者。
2.5 肺癌的治疗
CPFE合并肺癌的总体治疗方法与其他人群相似,条件许可的情况下优先选择手术切除(如Ⅰ期、Ⅱ期非小细胞肺癌),不具备手术条件时可考虑其他治疗方法(如化疗、靶向药物、放疗和姑息治疗)[33]。尽管可选择的治疗手段多种多样,但是相对而言CPFE合并肺癌患者在治疗过程中并发症的发生率通常更高,如手术切除后的急性肺损伤、ILD急性加重,放疗、靶向治疗、免疫治疗和化疗等相关的肺损伤发生率均明显高于非CPFE患者。目前指导风险评估的数据有限,但是也有研究发现,术中尽可能地保留肺容积、改进麻醉、采用立体定向放射治疗等都可能在一定程度上降低这些风险。
3、临床试验方面
3.1 终点的选择
关于CPFE的临床试验数量有限,这与疾病本身的病理生理学机制复杂有关。FVC是ILD相关临床研究中常用的观察终点,经证实FVC与疾病进展和高死亡风险相关,但CPFE中FVC的相对稳定阻碍了其作为观察终点在临床试验中的应用[34]。DLCO因为受到疾病严重程度(即地板效应)、测量可变性等因素的影响,在临床研究中作为观察终点也存在诸多限制[35]。有研究建议可以考虑在CPFE的临床研究中采用复合终点(例如死亡、因呼吸系统疾病住院或FVC下降)[36]。有回顾性研究提示,超过12个月FEV1下降>10%可能可以预测CPFE患者死亡风险增加[37]。针对CPFE还需要更进一步的研究,现有的数据可能对未来临床试验的设计和执行具有重要意义。
3.2 IPF临床试验中的CPFE患者
FVC的动态变化是目前IPF临床试验的首选主要终点[38],但是FVC的变化可能会被同时存在的肺气肿影响。在尼达尼布治疗IPF的INPULSIS试验中,FEV1/FVC<0.7的患者也被排除在外[39]。一项事后分析发现,39.6%的患者合并肺气肿,38.8%的患者0.7<FEV1/FVC≤0.8;与安慰剂组相比,无论是否合并肺气肿或FEV1/FVC范围不同(0.7<FEV1/FVC<0.8或FEV1/FVC>0.8)[14],IPF患者的肺功能(FVC下降的速度)都能从尼达尼布治疗中获益。CPFE患者是否能从抗纤维化治疗中获益,抗纤维化治疗的疗效是否与CPFE的严重程度有关,仍然需要更多的临床研究来证实。
4、研究前景
多数呼吸专科医生或全科医生对COPD比较熟悉,但并不熟悉CPFE的诊断和治疗。临床诊断为COPD的患者中,在轻至中度气流阻塞的情况下,DLCO严重降低表明可能需要额外的检查,特别是胸部HRCT。虽然肺气肿本身可能导致DLCO不成比例地降低,但也应警惕同时存在CPFE的可能,特别是考虑到HRCT中间质性肺异常(interstitial lung abnormality,ILAs)发生率高(>60岁的吸烟者中约8%发现ILAs),且需要关注这些表现与限制性肺通气障碍的关系,比如在肺功能中限制性通气障碍可能掩盖气流阻塞的特征[40]。虽然目前胸部HRCT并非COPD患者必须完成的检查项目,但还是引发了更多临床医师和研究者的关注[41],越来越多的COPD患者接受了影像学检查,无论是为了肺癌筛查还是为了更进一步地诊断检查和治疗,比如支气管内瓣膜置入,在这种情况下,HRCT可能最先发现纤维化的存在。在COPD队列研究中也发现,存在ILAs的患者的临床结果比没有ILAs的患者更差,包括运动能力降低[42]和全因死亡率增加[43]。
在诊断CPFE后,需要进行进一步的病史采集和与诊断相关的检查,类似于ILD患者的诊断流程[44]。一般来说,肺气肿的存在可能预示着更差的预后和更高的PH发病率,未来的研究也需要评估这一人群的肺癌风险。与普通人群相比,IPF和COPD都增加了肺癌的风险,但CPFE(或ILAs和肺气肿)患者的肺癌风险可能超过肺气肿或单独的IPF患者[5,45],这类患者通常预后也较差[45]。
该研究共识工作组委员会提出了目前存在的几个需要解决的知识空白,包括:(1)CPFE的发病机制;(2)CPFE的病理表现、疾病行为和自然病程;(3)改进早期诊断的方法;(4)寻找潜在的治疗机会。表2列出了CPFE的研究重点。

5、小结
总体来说,CPFE的主要特征是胸部HRCT和组织病理学表现为肺纤维化和肺气肿共存(无论是何种类型的f-ILD)。同时,相关共病和并发症的发生率会增加(特别是PH和肺癌)。肺纤维化合并肺气肿与疾病进展的相关性,以及这两种疾病相互关联的发病机制决定了CPFE应当被视为一种综合征。尽管已经有一些关于CPFE的研究,但仍有许多重要的问题没有得到解答。ATS/ERS/JRS/ALAT研究共识明确了CPFE的研究定义和分类标准,并确定了主要的研究重点,对进一步概括疾病特征、了解发病机制、指导临床管理至关重要。
(参考文献略)
基金项目:中国医学科学院医学与健康科技创新工程(2021-I2M-1-023)
作者:胡怡楠 任雁宏 代华平;国家呼吸医学中心 呼吸和共病全国重点实验室 国家呼吸临床研究中心 中国医学科学院呼吸病学研究院 中日友好医院呼吸与危重症医学科,北京 100029;通信作者:任雁宏,Email:ryhong7561@sina.com
引用本文:胡怡楠,任雁宏,代华平.《肺纤维化合并肺气肿综合征ATS/ERS/JRS/ALAT研究共识》解读(二):定义、综合管理及未来研究重点[J].国际呼吸杂志,2023,43(11):1267-1273.DOI:10.3760/cma.j.cn131368-20231002-00199.
本文转载自订阅号「国际呼吸杂志」
原链接戳:
《肺纤维化合并肺气肿综合征ATS/ERS/JRS/ALAT研究共识》解读(一);
《肺纤维化合并肺气肿综合征ATS/ERS/JRS/ALAT研究共识》解读(二)
* 文章仅供医疗卫生相关从业者阅读参考
本文完
责编:Jerry


