病例介绍
现病史:患者近4个月咳嗽,干咳为主,伴活动后气短,无发热、胸痛。
既往史:弥漫大B细胞淋巴瘤,IIIEB期,5程DA-EPOCH(依托泊苷、泼尼松、长春新碱、环磷酰胺、多柔比星)联合利妥昔单抗治疗后。4程治疗评估PR。末次抗肿瘤治疗时间为起病前2周。
个人史:吸烟30年,日均10支香烟。否认粉尘接触史。
体格检查:浅表淋巴结不大,无杵状指,双肺肺底可闻及散在Velcro啰音。
辅助检查:
常规:动脉血气:pH 7.43, pCO2 35mmHg, pO2 42mmHg。血常规、肝肾功能、血沉、CRP正常。肺功能:限制性通气功能障碍伴弥散功能减低。
感染筛查:诱导痰病原学(-);G试验、GM试验、血CMV-DNA(-)。
免疫指标:ANA 、ANCA(-)。
影像学检查:
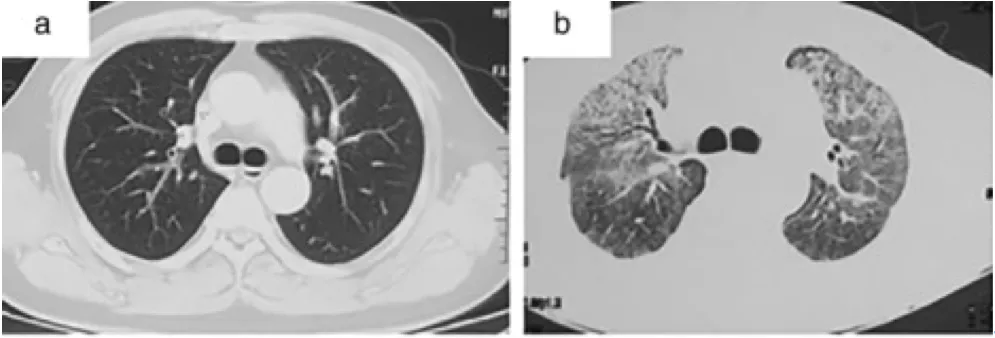
图1. (a) 4程抗肿瘤治疗后,呼吸道症状出现前:无明显异常。(b)起病4个月后:双肺弥漫磨玻璃影,纵隔窗无明显淋巴结肿大。
支气管镜:支气管粘膜未见明显异常。
治疗反应
先后给予莫西沙星、亚胺培南西司他丁抗细菌治疗无效。随后给予治疗剂量磺胺甲噁唑联合甲泼尼龙(160mg/d×3d,120mg/d×3d,80mg/d×5d,40mg/d×5d),症状改善。
停药1月后症状再次加重。
临床诊断是?(单选)
- 肺孢子菌肺炎
- 病毒性肺炎
- 淋巴瘤肺受累
- 系统性血管炎
- 药物相关间质性肺病
- 特发性间质性肺炎
进一步检查:
BALF病原学:涂片细菌、真菌、六胺银及抗酸染色均(-),细菌、真菌、分枝杆菌、奴卡菌培养(-),肺孢子菌DNA(-)。
BALF细胞分类:91%巨核细胞,6.5%淋巴细胞,0.5%嗜酸性粒细胞,2%中性粒细胞。
TBLB病理(图2):肺泡壁增厚,纤维组织增生,少量淋巴细胞浸润。
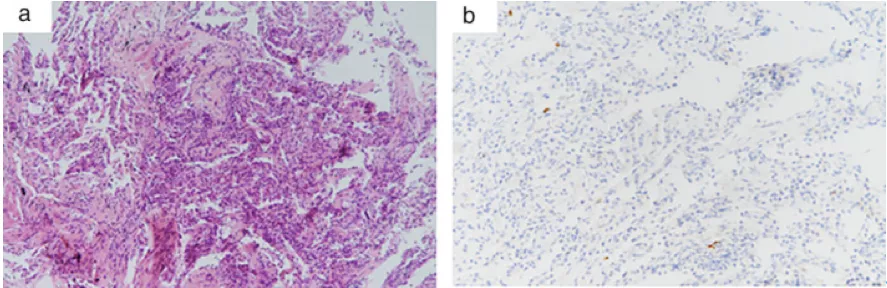
图2:(a) HE染色(×100):肺泡壁增厚,纤维组织增生,少量淋巴细胞浸润。(b)CD20免疫组化:肺内可见散在CD20+淋巴细胞。
最终诊断
利妥昔单抗相关间质性肺病
治疗与转归
给予泼尼松(0.8mg/kg·d)治疗3周,患者症状缓解,氧合改善,随后激素逐渐减量。用药6周、6个月、12个月复查胸部高分辨CT肺内磨玻璃影逐渐吸收(图3),肺功能好转。
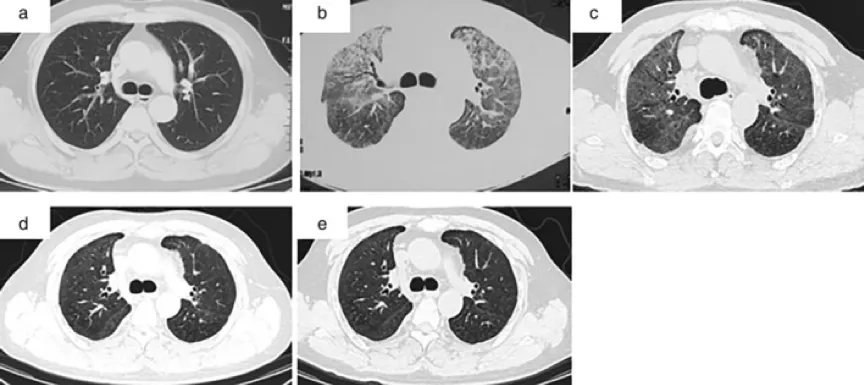
图3:(a) 4程抗肿瘤治疗后,呼吸道症状出现前:无明显异常。(b)起病4个月后:双肺弥漫磨玻璃影,纵隔窗无明显淋巴结肿大。(c-e): 糖皮质激素治疗后6周、6个月、12个月:肺内磨玻璃影逐渐吸收。
讨论
利妥昔单抗(Rituximab)
利妥昔单抗是一种人鼠嵌合抗CD20单抗,临床中广泛用于多种淋巴瘤和自身免疫性疾病的治疗。该药自1997年上市以来整体耐受性较好,其常见不良反应包括输注后出现皮疹、瘙痒等超敏反应及因免疫抑制继发感染。
利妥昔单抗相关间质性肺病
利妥昔单抗相关间质性肺病(Rituximab-induced interstitial lung disease, RTX-ILD)是该药一种少见的不良反应,其具体发病机制尚不完全清楚。本病起病中位疗程数4程,以呼吸困难、干咳、发热为主要临床表现,影像学特点为CT上肺内局限或弥漫的磨玻璃影,肺功能常见弥散功能障碍,病理改变以机化性肺炎为主,可伴有特异性间质性肺炎或寻常型间质性肺炎。多数患者在停用利妥昔单抗,并早期应用糖皮质激素治疗后可完全恢复,但亦有近15%的病死率。
在本例中,经多学科讨论,结合患者用药史、起病时间和对激素治疗的反应,排除感染、淋巴瘤复发等其他病因,最终诊断利妥昔单抗相关间质性肺病。
本例小结
对于接受含利妥昔单抗治疗方案的淋巴瘤患者,出现影像学上表现为双肺弥漫磨玻璃影的肺部病变时,应结合临床鉴别感染(尤其是肺孢子菌病、病毒性肺炎),左心衰(尤其使用了阿霉素类药物的患者)和淋巴瘤肺部受累,同时亦需注意利妥昔单抗相关间质性肺病的可能。
参考文献:
[1] 本病例以病例报告形式于2020年发表于Thoracic Cancer杂志:Sun YX, Shao C, Xu K, et al. Progressive dyspnea and diffuse ground-glass opacities after treatment for lymphoma with rituximab-containing chemotherapy: A case report. Thorac Cancer. 2020; 11(7): 2040-2043.
文字来源:孙宇新 邵池;文字整理:石穿
本文转载自订阅号「 协和呼吸」
原链接戳:当淋巴瘤患者出现肺部阴影(下)| 病例拾萃[30] · 协和呼吸
本文完
排版:Jerry


