引言
淋巴瘤是血液系统好发肿瘤,具有广泛累及全身各系统的特点,且异质性高,尤以肺部受累的淋巴瘤影像学表现复杂多样,可表现为实变、结节、网格影、双肺弥漫性病变等。其中又以双肺弥漫性病变表现的病因诊断最为艰难,易误诊。当有淋巴瘤基础的患者在治疗过程中出现双肺弥漫性改变时,如何明确病因?如何鉴别是淋巴瘤肺浸润还是继发肺部感染?或是化疗药物所致的肺损伤?这样的疑惑常常困扰临床医生。面对复杂的双肺弥漫性病变,该何去何从?如何让这类患者得到精准诊断及治疗?通过本病例的分享,或许对呼吸科临床医生在双肺弥漫性病变诊断中有所帮助。
患者曾明确诊断为「弥漫大B细胞淋巴瘤」,治疗后病情稳定……历时5年反复低热、活动后喘累,何因导致病情进展?
50岁的妇女唐某,因5年前一次上腹部疼痛到外院就诊,查体中发现其全身浅表淋巴结肿大。经淋巴结活检诊断为「弥漫大B细胞淋巴瘤」。外院先后按疗程给予其「NCID、NCOD、NCID、ECHOP、ECHOP、CHOP」方案化疗6次,治疗效果好,此后定期规律随访,自述一般情况良好,无复发迹象。
而1年多以前患者出现了纳差、乏力、左颈部淋巴结进行性肿大等症状,再次到外院行淋巴结活检后,证实仍为「弥漫大B细胞淋巴瘤」。外院血液科给予RCHOP(美罗华+长春地辛+环磷酰胺+表阿霉素+地塞米松)及CHOP(长春地辛+环磷酰胺+表阿霉素+地塞米松)方案治疗两次。化疗后,白细胞下降,长期维持在2-3*10^9/L之间。治疗期间,患者无反复发热、无喘累、咯血、腹泻、皮疹等症状。
近4个月前,患者无明显诱因再次出现反复低热,全天体温波动在37.5℃-38.3℃之间,伴间断干咳。无咯血、无体重下降、无盗汗。于社区医院输液治疗(抗感染具体方案不详),体温仍间断波动,因患者自觉不影响日常生活,未再进一步诊疗,化疗也同时中断。
至此次入我院治疗前1个多月,患者间断发热症状仍然存在,同时还出现活动后喘累症状,具体表现为走平路、洗漱即感到喘累,伴有频繁咳嗽,咳白色泡沫痰。病情加重1月以来,患者无咯血、盗汗,无胸痛、胸闷、夜间阵发性呼吸困难,无腹泻、腹痛,无恶心呕吐,无尿频、尿急、尿痛,体重无明显变化。为进一步治疗收入我科。
查患者既往史:否认除淋巴瘤以外的其他疾病史;个人史:无吸烟、饮酒史、无食物或药物过敏史;家族史:家人体健,兄弟姐妹无类似疾病史,否认家族遗传性疾病史。
入院后进行了血气分析提示为:PH7,40,PO2 52mmHg、PCO2 34mmHg、BE 2.6mmol/L、Lac 0.8mmol/L、SPO2 91%(鼻导管吸氧3L/min)。查体情况为:神志清楚,T 39.0℃、R 27次/分、BP102/60mmHg、HR 112次/分、SPO2 92%,口唇无紫绀,双肺呼吸音清,闻及湿啰音,胸膜摩擦音,无哮鸣音,心腹未见明显异常,双下肢不肿,浅表淋巴结未扪及肿大。辅助检查情况为:血常规示白细胞2.5*10^9/L、N 79.2%、L12%,ANA1:100,PCT 0.25ng/ml,CRP 77.10mg/L,血沉 28mm/h,肝肾功、电解质无异常,类风湿因子正常,抗核抗体及ANCA阴性,血癌谱正常,二便常规正常,输血前检查正常,肌酶谱正常,心肌酶谱及BNP正常。完善胸部CT见:双肺弥漫性病变。
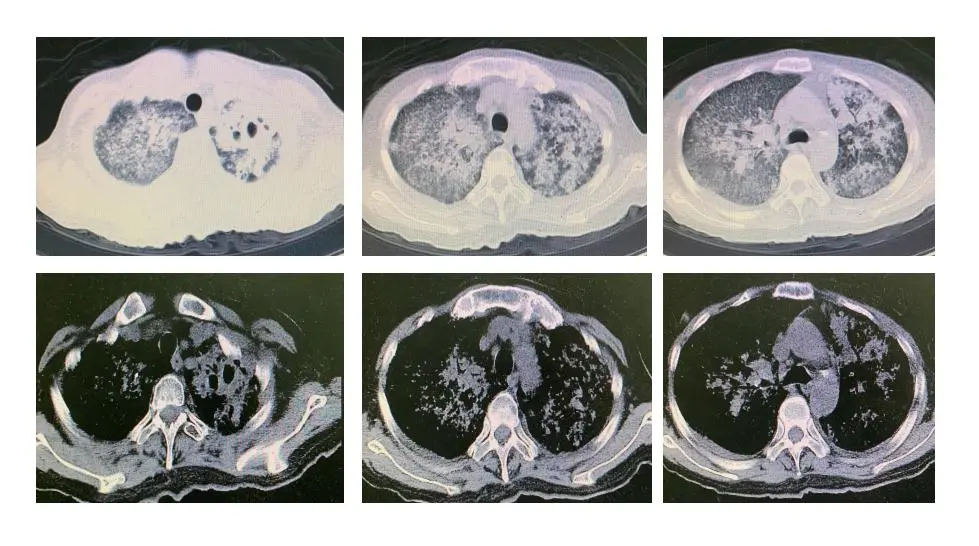
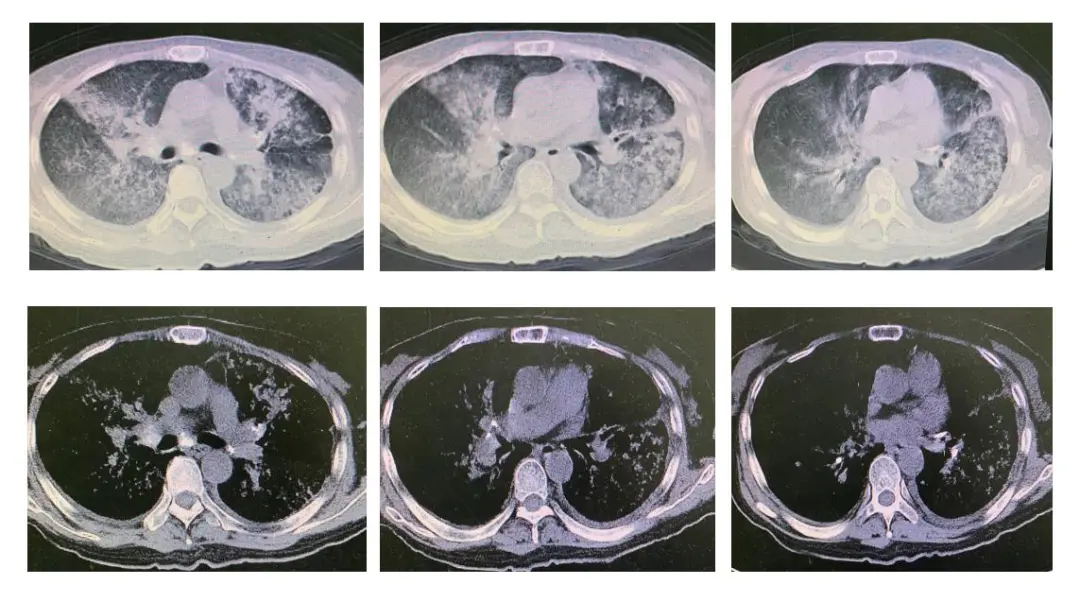
多手段鉴别诊断依然未明确病因,患者病情急转直下,呼吸衰竭不断加重……总结特点重点排查,如何制定下一步治疗方案?
双肺弥漫性病变常常是困扰呼吸科医生的难题,其病因复杂、病情危重、短时间内情况急转直下甚至危及生命,往往让临床医生在诊断及鉴别诊断之间绞尽脑汁。针对该患情况,下一步治疗方案该如何制定?如何明确病因?我们迅速展开了组内讨论分析。综合整理入院后相关病史资料,总结有以下几方面特点:1、有明确的血液系统肿瘤化疗后导致免疫力低下基础;2、有中断化疗后血液系统肿瘤进展的可能性;3、在前两点的基本前提下患者存在较长时间的慢性发热,且近1月来喘累症状明显,肺部影像学呈现弥漫性累及特点。4、入院后CRP、PCT、中性粒细胞百分比升高,入院前曾给予抗感染治疗未能稳定病情。
综合上述分析,我们将排查重点放在了以下几方面:
(1)感染性病变?结合慢性发热及影像学表现,首先考虑感染性病变,病原菌筛查集中在结核、真菌、少见病原菌、病毒之中,具体类型有待相关检查进行鉴别。
(2)淋巴瘤肺浸润?患者因发热中断化疗4个月,提示该患者在淋巴瘤复发后的整体治疗疗程不足,需要进一步鉴别淋巴瘤是否在中断治疗后出现进展,可同时请血液科会诊协助诊断。
(3)化疗药物肺损伤?查体摩擦音、CT提示双肺弥漫性病变、血气分析显示I型呼衰、使用美罗华及化疗药物所致慢性肺损伤需同时鉴别。
为证实分析,进一步完善相关检查:PPD皮试,血培养,痰细菌真菌涂片及培养,反复痰找脱落细胞,痰找抗酸菌,痰结核培养,呼吸道病原学9项检测,EB病毒筛查,巨细胞筛查,甲乙流筛查,骨髓穿刺,必要时需考虑肺组织活检。在等待结果的同时,予以亚胺培南西司他丁钠1g Q8h、万古霉素 1g Q12h、伏立康唑 200mg Q12h静滴病原体广覆盖,乙酰半胱氨酸片600mg tid 口服,稳定内环境,加强营养支持等治疗(为避免激素对检查结果的影响我们暂未使用),期待通过经验性广覆盖治疗策略先稳定体温,延缓肺部病灶进展,为患者的救治提供更多机会。
几日后的相关检查结果回示:PPD皮试阴性,血培养厌氧瓶及需氧瓶均无阳性发现,5次痰细菌真菌涂片及培养阴性,3次痰找脱落细胞未见癌细胞,3次痰找抗酸菌阴性,结核培养结果暂未出,呼吸道病原学9项阴性,EB及巨细胞病毒检测在正常范围,甲乙流筛查阴性,骨髓穿刺结果:骨髓增生欠活跃,组织细胞2%。
请血液科会诊考虑:骨髓中未见淋巴瘤特征性表现,但结合患者基础疾病淋巴瘤肺浸润仍不能排除,建议行肺活检。与此同时,再次复查血常规见:白细胞1.8*10^9/L、N 88.2%、L14%;PCT 0.89ng/ml、CRP >100mg/L.观察患者治疗后每日体温变化,体温高峰呈现下降趋势,全天体温徘徊在37.5-38.1℃之间,全天仍未能达到正常状态。更加令人不安的是,此时患者自觉呼吸困难症状无缓解,卧位翻身时即感呼吸困难加重,再次复查血气分析(5L/min面罩吸氧)情况下:PH7,45,PO2 56mmHg、PCO2 37mmHg、BE -2.2mmol/L、Lac 1.2mmol/L、SPO2 90%,呼吸衰竭进一步加重。
一系列「阴性」结果让诊断回到「原点」……我科首例重症病人TBCB术,难点在哪?需要把握哪些要点?
当进行完一系列相关鉴别诊断后,得到了一连串的「阴性」结果,令人「沮丧」。这时我们意识到,广覆盖抗感染的结果似乎不尽人意,而患者的病情在我们关注下仍在悄无声息地进展,诊断不仅几乎回到了「原点」,还让我们陷入了进退两难的境地。到底是治疗疗程不足还是病原菌仍未覆盖?或是淋巴瘤的进展未能被证实?又或者是已发生化疗药物不可逆转的肺功能损害?此阶段如何冲出困境,逆转劣势?是进行二次讨论的主要目的。
仔细回顾前期治疗过程,让我们陷入困境的是「期待有阳性结果的鉴别诊断却无一例外均为阴性」、「广覆盖的治疗方式未能让体温恢复正常似乎没有获得预期效应」。淋巴瘤、从未遇见过的病原菌、药物性肺损伤,三种情况都不能排除。无论哪种情况,目前迫切需要拿到核心证据。患者每况愈下的病情就像悬在我们头顶上的「达摩克里斯之剑」,时时刻刻提醒着时间不多。但偏偏这时难题却不断出现。二次讨论后,我们决定为患者进行经支气管冷冻肺活检(Transbronchial Cryobiopy,TBCB),期待从病理层面以及组织培养、支气管镜灌洗液等方面提供更多有利证据找到病因。但以患者目前的呼吸状况是否能耐受手术并且经受住术后任何风险的考验?二次组内讨论后的当天下午,紧急召开多学科MDT,麻醉科、影像科、血液科、感染科、呼吸科、胸外科共同就患者病情进行分析及充分评估,结合患者呼吸衰竭的状况,本次手术的难点在于:极有可能患者已存在缺氧导致的潜在其他脏器损伤。因此,活检过程应尽量迅速、微创,最大程度地保证活检过程的安全性,降低风险。
如何解决好难点?需要把握哪些要点?MDT后最终建议选择TBCB,在经与患者家属充分沟通得到同意后,一是建议在手术室在麻醉监护下建立硬质支气管镜通道下进行;二是同时对术中、术后可能的风险或并发症进行预防及制定相应预案,尤其是注意取样部位(避免离胸膜太近);三是将取样数量控制在4块以下,尽量避免气胸、大出血发生;四是保证组织标本的无污染,避免院感导致疾病加重风险。我们在术前严格按照软式内镜洗消规范,对气管镜进行了消毒,对冷冻探头给予低温等离子灭菌。手术医护人员严格执行外科手消毒,穿无菌手术衣,戴外科口罩、帽子,使用一次性医用手术手套。
次日,该患在手术室接受了硬质支气管镜下冷冻肺活检术。术中经历哪些过程?有哪些要求必须达到?1、高频通气及呼吸机联合辅助呼吸下,将该患者SPO2维持在93%-95%,心率维持在89-117次/分之间,动脉血压持续稳定在89-126/55-69mmHg范围内;2、镜下在左下叶背段进行支气管肺泡灌洗,再将冷冻探头分别送入右上叶后段各亚段离胸膜下2cm病灶处冷冻4s,分别获得大小约4mm-6mm的活体肺组织4块;3、取出后的组织块被装入无菌标本收集瓶,分别送检病理(含免疫组化及特殊染色)、细菌及真菌培养;4、术中出血量约20ml,每次冷冻活检后听诊查体均呼吸音对称,确保无气胸体征;5、麻醉复苏后将患者转入RICU观察24小时,拍摄床旁X片确保无气胸及胸腔积液。直至术后3天内确保患者无咯血,TBCB术顺利完成。
这次手术是我团队在全国开展首例TBCB术后的第二例TBCB肺活检术,也是我科首例重症病人TBCB术。
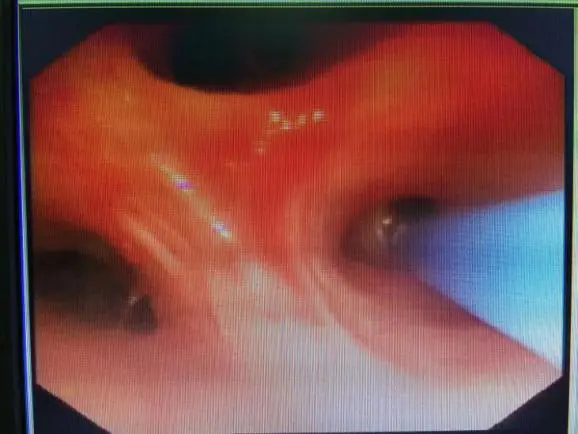
右上叶后段TBCB术
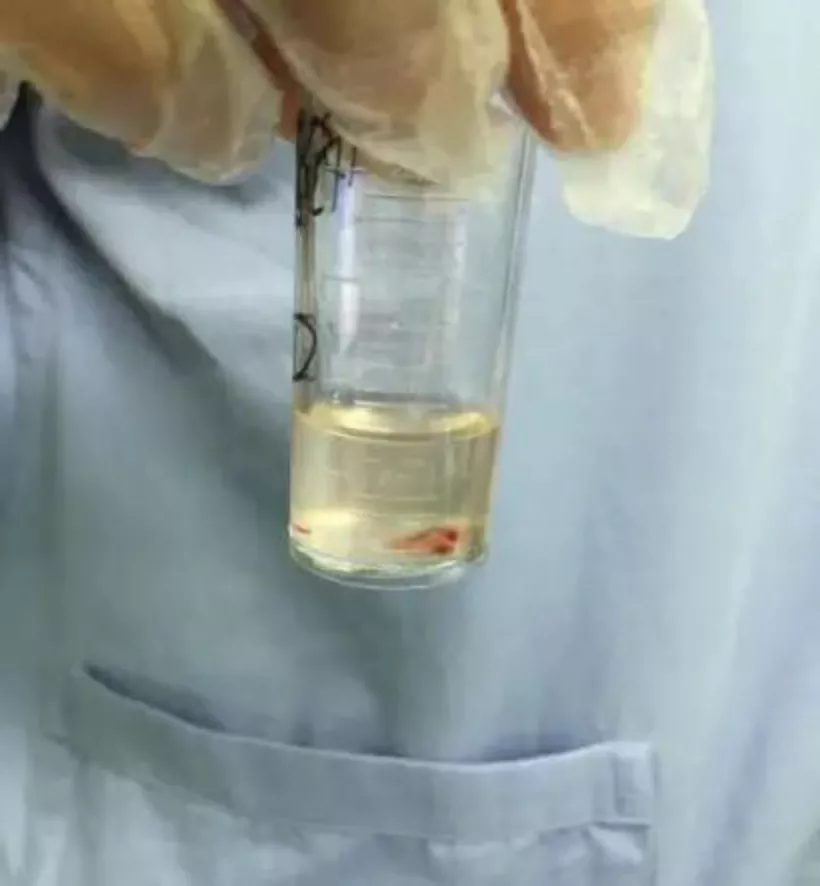
TBCB获得的肺组织标本
感染性因素或为致患者双肺弥漫性病变主要病因?3种病原微生物系「团伙作案」?这种菌天然耐药,是淋巴瘤的「另类」朋友?
活检术后第3天,支气管镜灌洗液结果提示:抗酸菌及脱落细胞阴性,GM试验及灌洗液培养阴性;灌洗液结核培养结果未回。
活检肺组织培养结果:无真菌生长,培养出血链球菌(氯霉素耐药)、粪肠球菌(克林霉素、喹努普汀/达福普汀耐药、万古霉素敏感)、假似肠膜明串珠菌。
病理结果提示:肉芽肿性炎、坏死物及少许玻变组织;免疫组化:CK(-) EMA(-) CD68(+)Ki67 5%(+)PAS(-)CD45(+)CD20(-)CD3(+);PAS染色(-)、抗酸染色(-)、TB-DNA(-)。
病理结论未提示淋巴瘤特征,免疫组化结果也排除了淋巴瘤表达特点,淋巴瘤肺浸润的支持依据不足。在病理结论中未提示间质性改变特点这与药物导致肺纤维化的表现不符。
根据上述结果,回归病因分析,我们考虑感染性因素是导致患者本次双肺弥漫性病变的主要病因。根据TBCB结果,对患者的组织培养结果进行分析:对于同时培养出的3种病原微生物,它们是「团伙作案」还是其中某位才是「始作俑者」呢?这一位「新朋友」---假似肠膜明串珠,它会是致病菌吗?
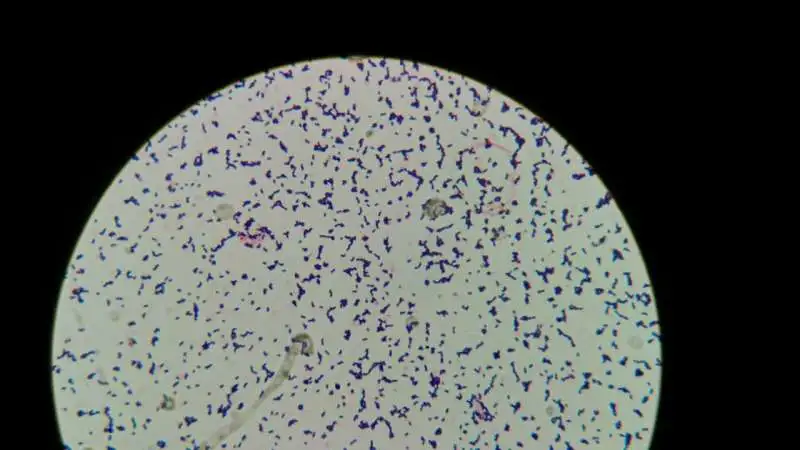
假似肠膜明串珠菌显微镜下表现(蓝紫色)
首先要明确什么是「假似肠膜明串珠菌」?明串珠菌是一种革兰阳性、兼性厌氧、无动力、通常表现为过氧化氢酶阴性的球杆菌,属链球菌科,由肠膜明串珠菌和其他7个种组成包括L. gelidum(冷明串珠菌)、L. carnosum(肉明串珠菌)、L. fallax(欺诈明串珠菌)、L. citreum(嗜柠檬酸明串珠菌)、L. argentinum(阿根廷明串珠菌)、L. pseudomesenteroides(假似肠膜明串珠菌)和L. lactis (乳酸明串珠菌)。
明串珠菌属常见于乳制品、发酵、酿酒及制糖工业中,在胃液、肠道、阴道分泌物中偶可分离出,因其细胞壁结构是L-丙氨酸-L-丙氨酸,故对于可以结合D-丙氨酸-D丙氨酸的万古霉素天然耐药。明串珠菌通常不致病,为机会致病菌,一旦引起人体感染时通常以败血症多见,还可引起肺炎、腹膜炎、进入脑脊液可导致脑膜炎、进入胸腔可引起胸腔积脓等。据此前文献复习目前鲜有已报道的明串珠菌致病文献中以败血症表现居多,肺炎表现尚属于首例。查阅热病及以往报道显示该菌通常对青霉素、氨苄青霉素、大环内酯类、氨基糖甙类、克林霉素敏感。
这种菌对万古霉素具天然耐药特性,在未被诊断前给予患者的初始经验性治疗过程中可能加剧了该菌群失调,促进其生长及感染?
对该病例进行回顾性分析:首先,患者有淋巴瘤基础,白细胞长期处于低水平状态,免疫力低下,具有明串珠菌感染的宿主因素;其次,明串珠菌不在鼻腔、口腔或呼吸道内定植,经气管镜操作导致样本污染概率较低。反复询问患者否认本次就诊前曾出现消化道症状或呕吐误吸;第三,通过TBCB所取到的深部肺组织来看,培养结果虽三种致病菌共存,但该患者入院后使用万古霉素及亚胺培南西司他丁钠治疗,抗菌谱已经覆盖「粪肠球菌及血链球菌」,其药敏结果也提示粪肠球菌对万古霉素敏感。相反,对于假似肠膜明串珠而言,由于其对万古霉素天然耐药特性,在未被诊断之前给予患者初始经验性治疗的过程中可能加剧了该菌群失调,促进了明串珠菌生长及感染。
我们又联合多学科再次MDT,根据热病及培养的药敏结果,讨论建议:将药物调整为「青霉素 400万u 静滴 q12h、万古霉素500mg 静滴 q12h」继续治疗,观察药物使用过程中的疗效及副反应,择期复查胸部CT。
在调整治疗方案后,患者家属要求转入血液科,为淋巴瘤后续治疗做准备。随访该患者转入血液科后沿用上述方案体温逐渐下降恢复正常。但遗憾的是,该患者终因前期病程持久,机体较长时间持续缺氧,双肺弥漫病变范围广,出现严重的酸中毒,心肌、肝功损害,凝血功能异常,导致多脏器功能衰竭,再次转入ICU仍未能挽救患者生命。
思考和讨论
通过此病例的诊断过程,我们得到以下启示:
1、双肺弥漫性病变是呼吸科经常遇到的疑难危重症,其病因诊断常常关乎患者的预后,尽早介入干预有助于协助临床医生获取有价值的标本,尽早实现精准诊断和早期精准治疗。
2、对于感染患者选用超广谱抗菌素需要严格把握指针,特别是针对免疫低下人群选药时需考虑到机会致病菌感染的风险,经验性选药固然是救治患者的重要手段,但当病情发展与药物疗效不匹配时需尽早变换思路,避免默守陈规延误救治时机。
3、对于免疫力低下合并慢性发热的人群,在病原体判断方面,除常见细菌、真菌、病毒、结核感染外,特别需警惕少见、罕见病原菌和特殊病原菌感染可能,在诊断及治疗过程中尽量避免单纯的经验性治疗,应尽量通过痰液、体液、血液、支气管镜、或肺穿刺活检、甚至介入性手段取得有价值标本送检。
4、TBCB术操作安全性好,即使在双肺弥漫性病变ARDS患者中,只要及时掌握合适时机进行操作,仍能有效获取标本,对诊疗有十分重要的意义,值得推荐。
5、由于明串珠菌发病实属罕见,其发生机会性致病机制以及影像学特征尚不明确,我们欢迎有经验的同道们提供宝贵建议,也期待在未来的医学发展中对该菌有更深入的了解。
专家介绍

郭述良
重庆医科大学附属第一医院呼吸与危重症医学科(国家临床重点专科)主任;重庆市医师协会呼吸医师分会会长;重庆市医院协会呼吸内科管理专业委员会主任委员。中华医学会结核病学分会常务委员,呼吸内镜专业委员会主任委员;中国医师协会呼吸医师分会介入呼吸病学工作委员会呼吸病血管介入学组组长;中华医学会呼吸病学分会介入呼吸病学组委员;中国研究型医院学会呼吸病学分会介入呼吸病学组副组长。

戴枥湾
主治医师,医学硕士,重医附一院呼吸与危重症医学科PCCM专培学员,2012年至今从事呼吸与危重症医学科的临床、教学、科研工作,熟练掌握呼吸系统常见病和疑难危重病人的救治,能独立完成呼吸介入1-3级手术操作;擅长呼吸疑难危重症病人的综合诊疗。多次获重庆医科大学第一临床学院“受好评教师”。多次参加国内及国际会议,并在大会中投稿及发言。发表中英文学术论文数篇。主持省部级课题一项。亚专业方向:呼吸康复。

吴金星
副主任医师,医学硕士。1990年7月毕业于泸州医学院医疗系,1993年7月-1994年7月在西南医院心内科进修学习,2001年9月-2004年7月在重庆医科大学攻读心血管硕士学位。2016年9月~12月西安交通大学附属第一医院进修学习。从事临床工作30余年,擅长支气管镜、超声支气管镜、内科胸腔镜、全肺灌洗、支气管动脉介入治疗大咯血和肺癌灌注化疗等诊疗技术,尤其在支气管动脉介入治疗方面具有丰富的临床经验。多次获得好评教师,获得指导全国大学生临床技能大赛二等奖,发表教学论文1篇。发表学术论文15篇,其中SCI论文2篇,获得实用新型专利2项,获得国家发明专利1项。现为中华医学会结核分会呼吸内镜介入专委会常务委员,重庆市呼吸介入病学组委员。重庆市卫计委科技成果二等奖一项。主要研究方向:肺病介入及肺血管疾病。

周蜜
主治医师,在读博士。2013年毕业于重庆医科大学临床医学七年制专业,现参加重医一院呼吸与危重症医学科PCCM培训项目。擅长呼吸内科常见疾病如肺炎、慢性阻塞性肺病、支气管哮喘、肺癌等疾病的诊断及治疗,擅长呼吸内科危重症患者的救治,擅长呼吸康复治疗。目前从事肺癌、肺康复的研究,撰写中文论文多篇,发表SCI论文6篇。
本文完
采写编辑:冬雪凝;排版:Jerry


