研究背景
碳青霉烯类耐药肠杆菌目细菌(carbapenem-resistant Enterobacterales,CRE)是医院获得性感染的主要致病菌。定义为对任意一种碳青霉烯类抗菌药物(包括厄他培南、美罗培南、多利培南和亚胺培南)耐药或者产碳青霉烯酶,此外对亚胺培南天然耐药的细菌(如变形杆菌属、普罗威登斯菌属、摩氏摩根菌等),须除对亚胺培南以外的其他碳青霉烯类抗菌药物耐药。CRE耐药广泛、耐药性传播快、病死率高、临床可用的抗菌药物有限,已成为临床面临的「超级挑战」。近年来,CRE血流感染的发生率呈上升趋势,给临床抗感染治疗带来了更为严峻的挑战。
北京大学人民医院王辉教授团队(第一作者周朝娥)采用前瞻性多中心观察性研究,收集了我国2019年9个省18家医院208例CRE血流感染患者的病例信息以及相对应CRE菌株,评估了CRE血流感染发生脓毒症或脓毒性休克以及死亡的相关危险因素和临床抗菌治疗预后,为我国CRE血流感染的防控与治疗提供重要的参考依据。此研究发表在Infection and Drug Resistance杂志上。
研究方法
本研究为前瞻性观察性研究,严格按照纳入标准(1.CRE血流感染;2.年龄≥18岁)和排除标准(1.年龄<18岁;2.关键数据缺失;3.多细菌混合感染),共收集了我国2019年1月至12月9个省18家医院208例CRE血流感染患者病例信息和相对应的CRE菌株,菌株做Illumina测序。应用logistic回归分析CRE血流感染发生脓毒症或脓毒性休克以及30天病死率的危险因素,Log rank test统计方法评估临床抗菌药物治疗预后。
主要结果
1、CRE血流感染30天病死率的相关危险因素分析
我国CRE血流感染30天病死率为46.2%(96/208)。单因素Logistic回归分析结果示跟CRE血流感染30天病死率相关的危险因素有:Charlson合并症指数高评分(p=0.002)、致病菌替加环素MIC≥0.5mg/L(p=0.009)、CRE分离时患者住在ICU(p=0.044)、动脉插管(p=0.023)、中心静脉置管(p=0.030)、入院前30天抗生素暴露史(p=0.035)、经验性使用替加环素(p=0.030)、Pitt菌血症评分高(p=0.001)、发生脓毒症或脓毒性休克(p<0.001)以及短疗程抗菌药物治疗(p<0.001)(Table 1)。
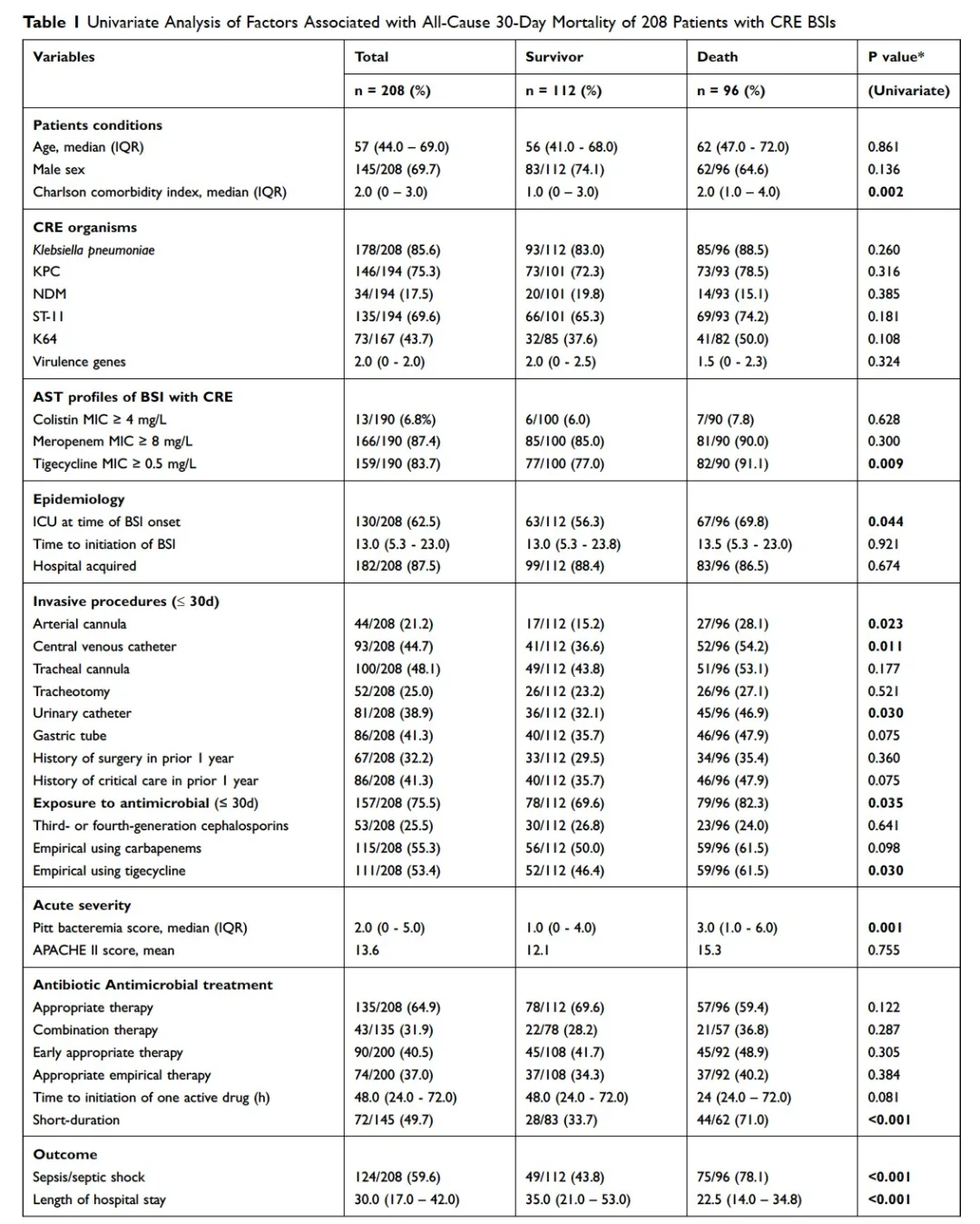
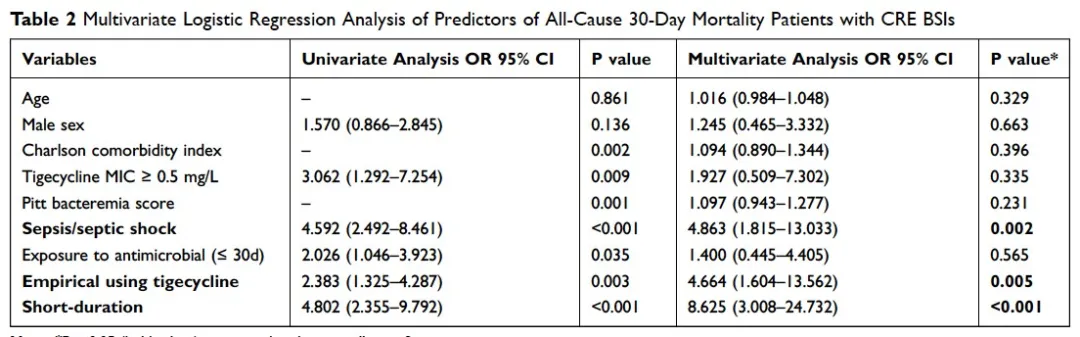
多因素Logistic回归分析结果示发生脓毒症或脓毒性休克(OR 4.863,95% CI 1.815–13.033,p=0.002)、经验性使用替加环素(OR 4.664,95% CI 1.604–13.562,p=0.005)以及短疗程抗菌药物治疗(OR 8.625,95% CI 3.008–24.732,p<0.001)是CRE血流感染30天病死的独立危险因素(Table 2)。
2、CRE血流感染患者发生脓毒症或脓毒性休克的相关危险因素分析
单因素Logistic回归分析结果示跟CRE血流感染发生脓毒症或脓毒症休克相关的危险因素有:动脉插管(p=0.019)、长期留置鼻导管(p=0.012)、CRE感染前1年内急重症住院史(p=0.027)、Pitt菌血症评分高(p=0.009)以及ST11–KL64(多位点序列分型为ST11,血清分型为KL64)的肺炎克雷伯菌感染(p=0.008)(Table 3)。
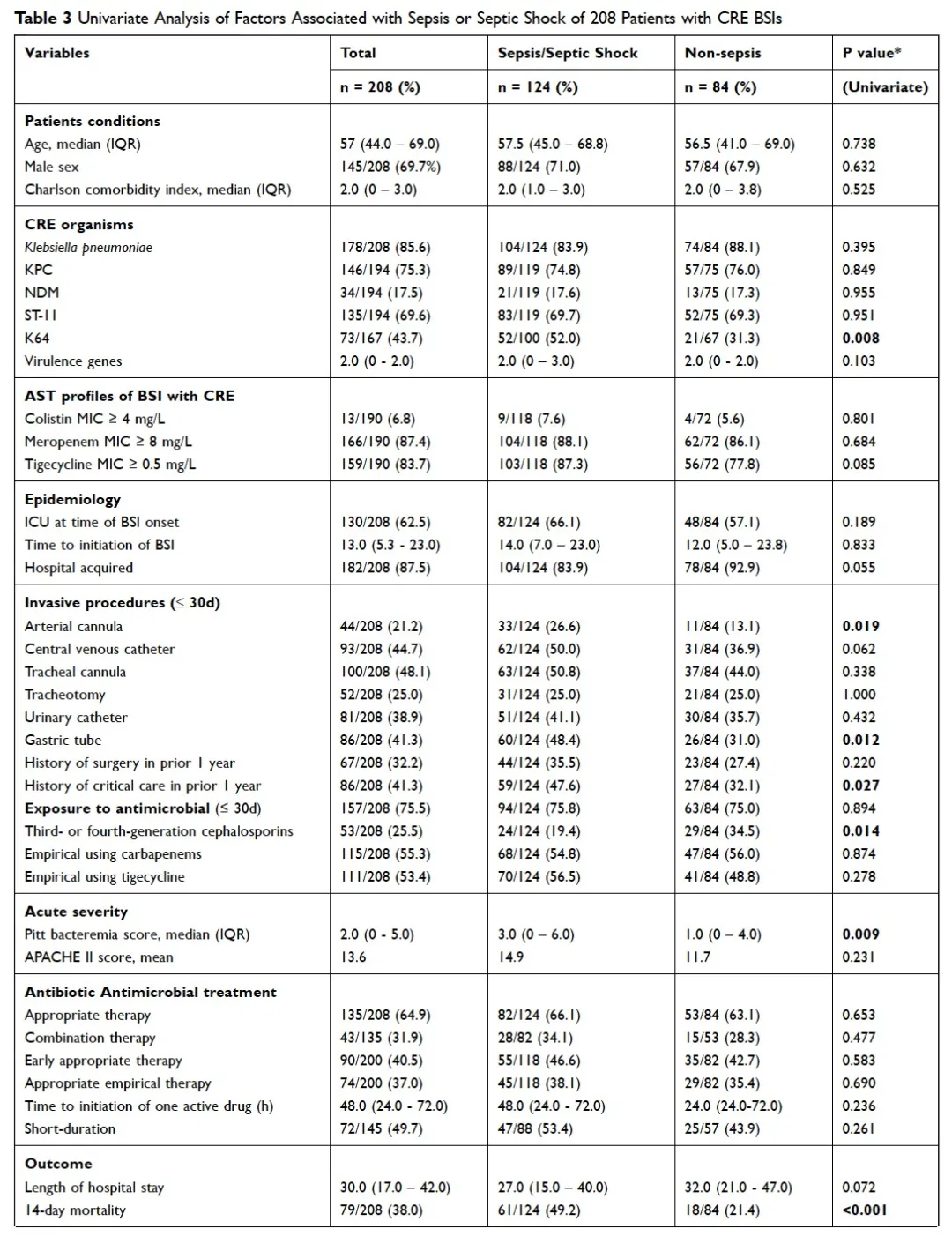
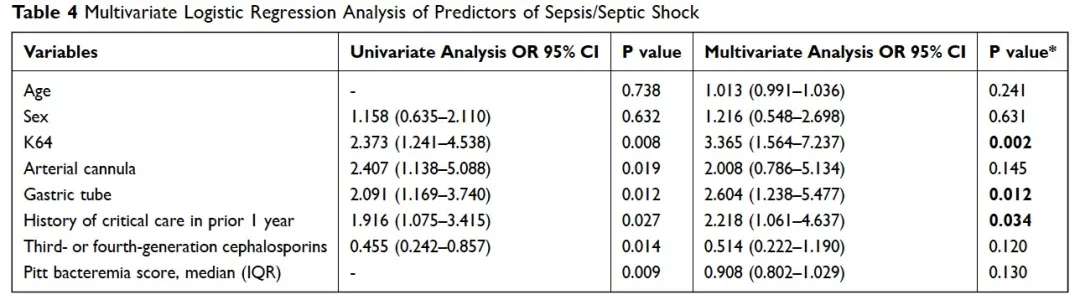
多因素Logistic回归分析结果示ST11–KL64的肺炎克雷伯菌感染(OR 3.365,95% CI 1.564–7.237,p=0.002)、长期留置鼻导管(OR 2.064,95% CI 1.238–5.477,p = 0.012)以及CRE感染之前1年内有急重症住院史(OR 2.218,95% CI 1.061–4.637,p=0.034)是CRE血流感染发生脓毒症或脓毒性休克的独立危险因素(Table 4)。
3、CRE血流感染菌株特点
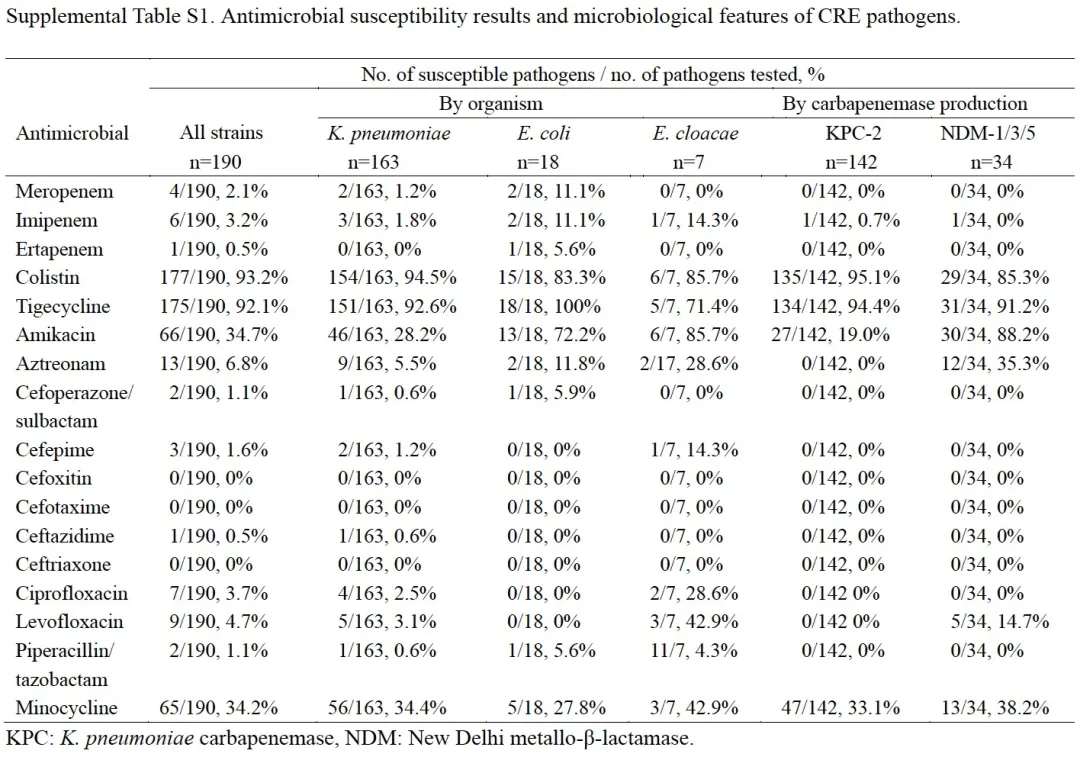
在CRE血流感染的菌株中,肺炎克雷伯菌是主要致病菌(85.6%,178/208)。耐药基因型以blaKPC-2最为常见(75.3%,146/194),其次为blaNDM(17.5%,34/194),最主要的多位点序列分型为ST11(69.6%,135/194)。在肺炎克雷伯菌中,最常见的血清分型为KL64(43.7%,73/167),其次为KL47(30.5%,51/167)。各种抗菌药物敏感率如Table S1所示:多黏菌素(93.2%)、替加环素(92.1%)、阿米卡星(34.7%)、米诺环素(34.2%)、氨曲南(6.8%)、左氧氟沙星(4.7%)、环丙沙星(3.7%)、亚胺培南(3.2%)、美罗培南(2.1%)和厄他培南(0.5%)。
替加环素MIC≥0.5mg/L菌株感染患者30天病死率高于替加环素MIC<0.5 mg/L菌株感染患者(p=0.009),美罗培南和多黏菌素MIC水平高低与患者预后无关。ST11–KL64肺炎克雷伯菌感染患者发生脓毒症的概率高于ST11–KL47肺炎克雷伯菌(p=0.050)和其他血清分型菌株感染(p=0.016)。
4、临床抗菌药物治疗预后
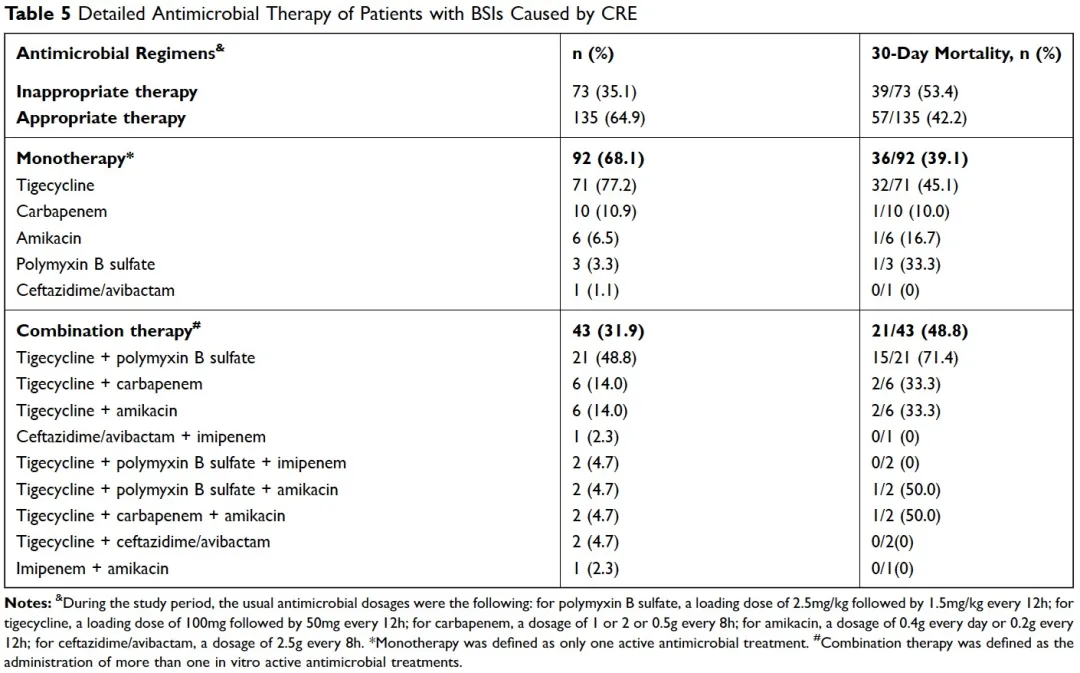
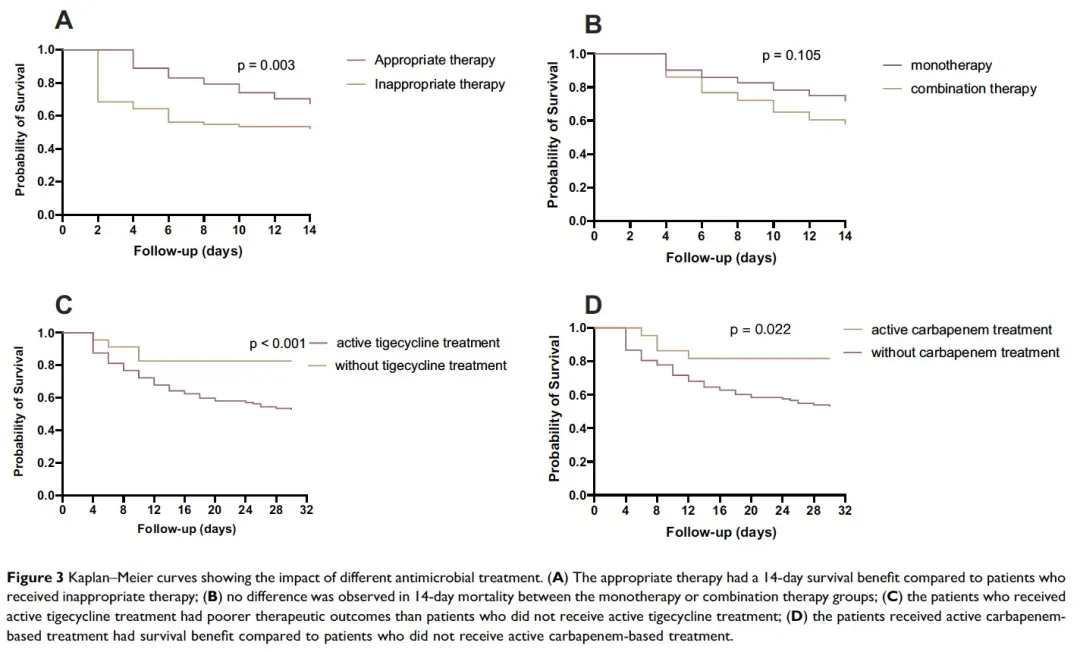
CRE血流感染患者接受具体的抗菌药物治疗及预后见Table 5。在208个CRE血流感染患者中,135个患者接受恰当的抗菌药物治疗,73个患者接受不恰当的抗菌药物治疗,接受恰当的抗菌药物治疗患者14天病死率显著低于接受不恰当的抗菌药物治疗患者(p=0.003)(Figure 3a);92个患者接受抗菌药物单药治疗,43个患者接受抗菌药物联合治疗,二者14/30天生存率无明显差别(p=0.105)(Figure 3b);112个患者接受活性抗菌药物替加环素治疗,患者生存率略差于未用活性抗菌药物替加环素治疗的患者(p<0.001)(Figure 3c);碳青霉烯类抗菌药物对碳青霉烯类药物MIC≤8mg/L的菌株感染治疗效果优于碳青霉烯类抗菌药物MIC>8mg/L的菌株感染(p=0.022)(Figure 3d)。
CRE血流感染病死率高,感染源的控制、早期识别相关危险因素以及恰当的抗菌药物治疗是患者预后的关键。尽早的控制感染源是决定患者预后的主要因素。对于重症监护患者、血液肿瘤患者、侵袭性操作、免疫抑制患者、长期住院患者、肠道菌群失调患者以及抗菌药物不规范使用的患者需警惕CRE血流感染的发生。抗菌药物合理应用是患者预后的关键因素,经验性抗菌药物使用主要用于重症患者,既要根据当地可疑病原体合理地使用经验药物,也要努力进行快速的病因诊断以逐步降低病情。抗菌药物的靶向治疗应根据体外药敏结果及感染部位选择具有活性的抗菌药物治疗。联合用药仅限于脓毒症休克患者,而不常规用于其他严重感染或无循环衰竭的患者。抗菌药物降阶梯治疗旨在减少抗菌药物治疗的范围并减少抗菌药物耐药性的出现。足够的抗菌药物治疗疗程可防止临床治疗失败和复发,但不应超过所需的抗菌药物治疗疗程,治疗疗程的确定需考虑到患者自身的疾病严重程度、感染灶的控制以及附加感染等混杂因素的影响。
总之,我国CRE血流感染病死率高,尽早识别危险因素预防CRE感染以及感染后合理的抗菌药物治疗是改善患者预后的关键。
最后致谢CRE network全体成员!
参考文献: Zhou C, Jin L, Wang Q, Wang X, Chen F, Gao Y, Zhao C, Chen H, Cao B, Wang H. Bloodstream Infections Caused by Carbapenem-Resistant Enterobacterales: Risk Factors for Mortality, Antimicrobial Therapy and Treatment Outcomes from a Prospective Multicenter Study. Infect Drug Resist. 2021;14:731-742 https://doi.org/10.2147/IDR.S294282
作者:周朝娥 - 北京大学人民医院;审校:王启
本文转载自订阅号「京港感染论坛」(ID:PIDMIC)
原链接戳:【CRE专栏】CRE血流感染危险因素及临床抗菌治疗预后的前瞻性研究
本文完
排版:Jerry


