
一、病史简介
患者,男性,69岁,山东人,2024-02-01入住中山医院感染病科。
主诉:发热伴咳嗽咳痰5天。
现病史:
2024-01-28 无明显诱因下出现发热,Tmax 38.6℃,伴咳嗽、咳少许白粘痰、胸闷气促。01-30当地医院查WBC 2.85X10^9/L,N 82%;甲型及乙型流感、新型冠状病毒核酸均阴性,予退热药物口服,仍反复发热。
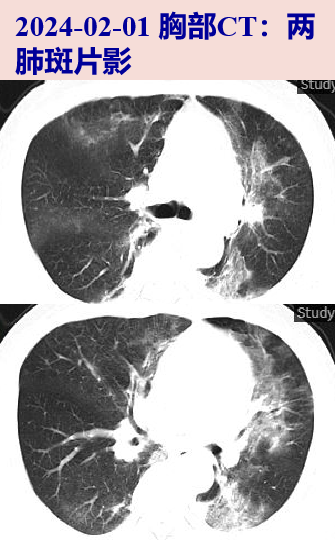
2024-02-01 至我院发热门诊,查WBC 3.25X10^9/L,N 83%,CRP 52.5mg/L;新型冠状病毒核酸阴性;呼吸道六联检:乙型流感RNA阳性,甲型流感病毒、鼻病毒、腺病毒、呼吸道合胞病毒、肺炎支原体核酸阴性;胸部CT:两肺斑片影,食管中段管壁略增厚,纵隔小淋巴结。
2024-02-01 为明确发热和肺部病灶病因收入中山医院感染病科。
既往史:2023-09确诊为食管鳞癌,予抗PD-L1(阿得贝利单抗)+白蛋白紫杉醇+奈达铂治疗6周期,2024-01-15起抗PD-L1单药治疗。高血压病史8年,最高150/90mmHg,因化疗后血压正常,目前未服用降压药物。
二、入院检查(2024-02-01)
【体格检查】
T:38.5℃ P:119次/分 R:22次/分 BP:122/67mmHg。神清,双肺未及明显干湿啰音,心律齐,未闻及心脏杂音,腹软无压痛,双下肢未见水肿。
【入院化验】
血常规:WBC 3.25X10^9/L,N 83.1%,Hb 131g/L ,Plt 122X10^9/L
血气分析(鼻导管5L/min):PH 7.54,PaCO2 39mmHg,PaO2 98mmHg,FiO2 239
炎症标志物:CRP 52.5mg/L,ESR 3mm/H,PCT 0.1ng/ml
心脏标志物:cTnT 0.017ng/mL,proNT-BNP 417pg/mL
生化:ALT/AST 176/144U/L,LDH 409U/L,Alb 32g/L,Cr 56μmol/L
D-二聚体 1.69mg/L
T-SPOT.TB:A/B抗原 0/0(阴性/阳性对照:0/195),G试验、GM试验、EBV/CMV-DNA均阴性;
细胞免疫:T淋巴细胞绝对计数 102cells/uL,CD4 55cells/uL,CD8 43cells/uL
肿瘤标志物、自身抗体均阴性
【辅助检查】
心电图:窦性心动过速,频发房性早搏。
心超:主动脉瓣钙化。
三、临床分析
病史特点:老年男性,食管恶性肿瘤化疗及抗PD-L1免疫治疗后,急性病程,主要表现为发热、咳嗽、胸闷气促,血白细胞降低、CRP升高,肺部CT见左肺为主的双肺斑片状模糊影,需考虑以下病因的鉴别诊断:
1、细菌性肺炎:社区获得性肺炎常见病原体包括肺炎链球菌、流感嗜血杆菌、卡他莫拉菌等,通常为急性病程,表现为高热、咳嗽、咳痰,伴有白细胞及炎症指标升高,胸部CT可见肺叶或肺段实变。该患者以发热伴咳嗽咳痰、胸闷气促为主要表现,血WBC降低(化疗后骨髓抑制可能),CRP升高,PCT正常,胸部CT表现为两肺多发散在模糊影,需考虑普通细菌感染,可通过痰细菌涂片、培养、mNGS及经验性抗感染治疗后评估疗效以协助诊断。
2、真菌性肺炎:本例患者急性起病,主要表现为发热咳嗽,既往肿瘤化疗及免疫治疗,胸部CT表现为两肺片状模糊影后,未见多发空洞等肺部真菌感染常见影像学改变,入院查G试验、GM试验阴性,真菌感染可能小, 但仍无法除外耶氏肺孢子菌(PJ)感染,需要结合痰涂片、培养,痰真菌三联检(曲霉菌属、新型隐球菌、耶氏肺孢子菌核酸检测)及痰NGS结果以明确。
3、病毒性肺炎:常见病毒包括流感病毒、新型冠状病毒、腺病毒等,该患者以发热、咳嗽咳痰起病,血白细胞、PCT不高,CRP升高,我院查乙流核酸阳性,需考虑病毒性肺炎,但乙流病毒通常毒力较低,引起肺炎较少,本例的胸部CT表现也似乎不支持流感肺炎表现。
4、非感染性疾病:如风湿性疾病、免疫相关性肺炎等,该患者表现为急性期发热、咳嗽咳痰,但血白细胞不高,炎症标志物仅CRP升高,两肺多发模糊影,但自身抗体阴性,且无皮疹、关节疼痛等表现,暂不考虑风湿性疾病;患者既往抗PD-L1抗体多次用药史,胸部CT见两肺散在阴影,如病原学检查阴性,结合后续抗菌药物等治疗效果评估,有助于明确诊断。
四、进一步检查、诊治过程和治疗反应
2024-02-01 查血培养,同时留取血、痰标本送检mNGS;予玛巴洛沙韦 40mg po st抗病毒,SMZ-Co 0.96g q8h*1d→q12h po(因肝酶升高减量)抗耶氏肺孢子菌,辅以保肝、补充白蛋白、碱化尿液、低分子肝素预防性抗凝等对症治疗;
2024-02-02 痰真菌三项(02-01采样):肺孢子菌DNA阳性,Ct值32.19;曲霉、隐球菌DNA阴性;痰涂片找细菌、真菌、抗酸杆菌阴性,Xpert.TB阴性;
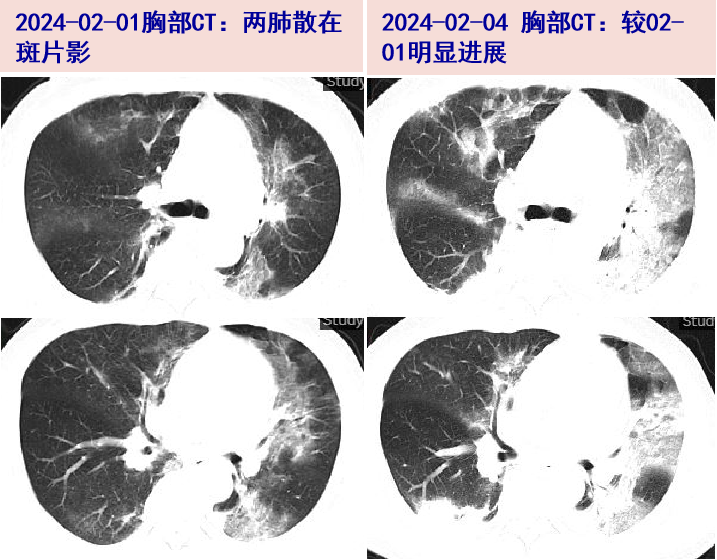
2024-02-03 Tmax 39.5℃,复查血气分析(鼻导管10L/min):PH 7.48,PaCO2 40mmHg, PaO2 99mmHg;P/F 220mmHg;血常规:WBC 2.56×10^9/L,N 84.9%;炎症标志物:ESR 38mm/H,hs-CRP 83.9mg/L,PCT 0.07ng/ml;ALT/AST 126/103U/L;低氧血症加重,复查新冠核酸及呼吸道六联检阴性;痰细菌、真菌培养(02-02采样):阴性;痰mNGS(02-01采样):检出大量流感嗜血杆菌核酸序列。胸部CT:两肺炎症渗出改变,两下肺部分实变,较02-01片明显进展。结合患者既往抗PD-L1抗体治疗史,考虑免疫治疗相关肺炎可能,合并细菌、真菌、PJ感染不除外,予高流量吸氧,加用甲泼尼龙40mg bid ivgtt,同时卡泊芬净70mg d1→50mg qd ivgtt,美罗培南1g q8h ivgtt,左氧氟沙星0.5g qd ivgtt抗感染;

2024-02-05 血mNGS:检出极少量耶氏肺孢子菌核酸序列

2024-02-06 血气(HighFlow 25L/min 氧浓度70%):PH 7.49,PaO2 71mmHg ;P/F 101mmHg,血常规:WBC 6.19×10^9/L,N 93%;炎症标志物:ESR 3mm/H,hs-CRP 38.6mg/L,PCT 0.07ng/ml ;ALT/AST 171/127U/L;血培养回报(02-01采样):阴性;痰真菌三项(02-02采样):肺孢子菌DNA阳性,Ct值30.41;痰mNGS(DNA+RNA):检出人类疱疹病毒7型。患者体温高峰下降,02-07停用卡泊芬净。

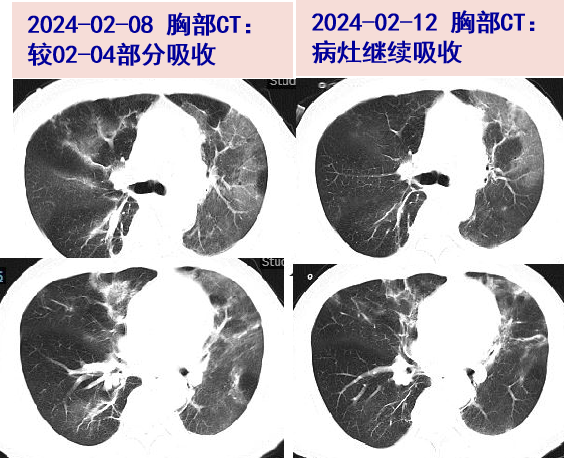
2024-02-08 胸部CT:两肺多发斑片、条片状模糊影,较02-04片部分吸收;调整为鼻导管吸氧,甲泼尼龙减量为40mg qd ivgtt,停用左氧氟沙星。
2024-02-09 体温平,咳嗽咳痰气促较前好转;血气(鼻导管6L/min):PH 7.49, PaO2 170mmHg ;P/F 377mmHg;血常规:WBC 5.93×10^9/L,N 77.4%;炎症标志物:ESR 18mm/H,hs-CRP 5.5mg/L,PCT 0.06ng/ml ;ALT/AST 165/68U/L;停用美罗培南。
2024-02-12 复查血常规:WBC 5.12×10^9/L,N 71.5%;炎症标志物:ESR 3mm/H,hs-CRP 2.4mg/L,PCT 0.05ng/ml;ALT/AST 122/56U/L;胸部CT:两肺散在斑片、条片状模糊影,较02-08片稍有吸收。
2024-02-13 甲泼尼龙调整为30mg qd ivgtt;复查痰真菌三项:阴性;停用SMZ-Co。
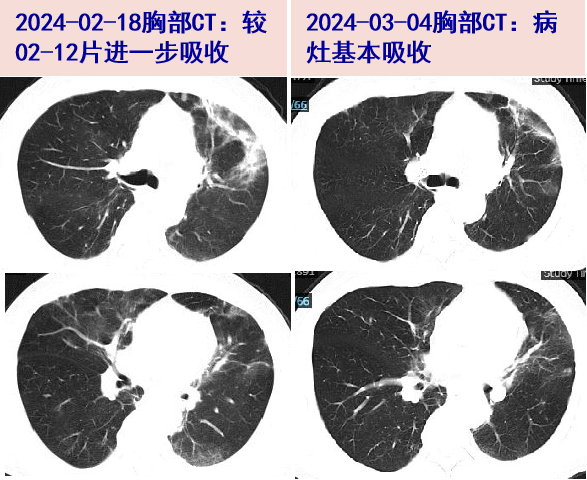
2024-02-17 甲泼尼龙减为20mg qd ivgtt;02-18血常规:WBC 4.25×10^9/L,N 71.7%;炎症标志物:ESR 5mm/H,hs-CRP 0.6mg/L,PCT 0.05ng/ml,ALT/AST 68/29U/L;胸部CT:两肺散在斑片、条片、结节状模糊影,较前进一步吸收;
2024-02-21 患者体温平,咳嗽、咳痰进一步好转,无活动后气促,予甲泼尼龙20mg qd po 出院。
出院后随访:
2024-03-04 出院后无发热、咳嗽气促等;甲泼尼龙20mg qd po*5d(02.22-02.26)→16mg qd po(02.27-03.04);我科门诊随访,患者无发热、咳嗽,SpO2 97%(不吸氧),复查血常规:WBC 6.65×10^9/L,N 71.5%;炎症标志物:ESR 4mm/H,hs-CRP 5.7mg/L;胸部CT:两肺少许斑片、条片、结节状模糊影,病灶基本吸收。甲泼尼龙减为12mg qd po,每2周减2mg。
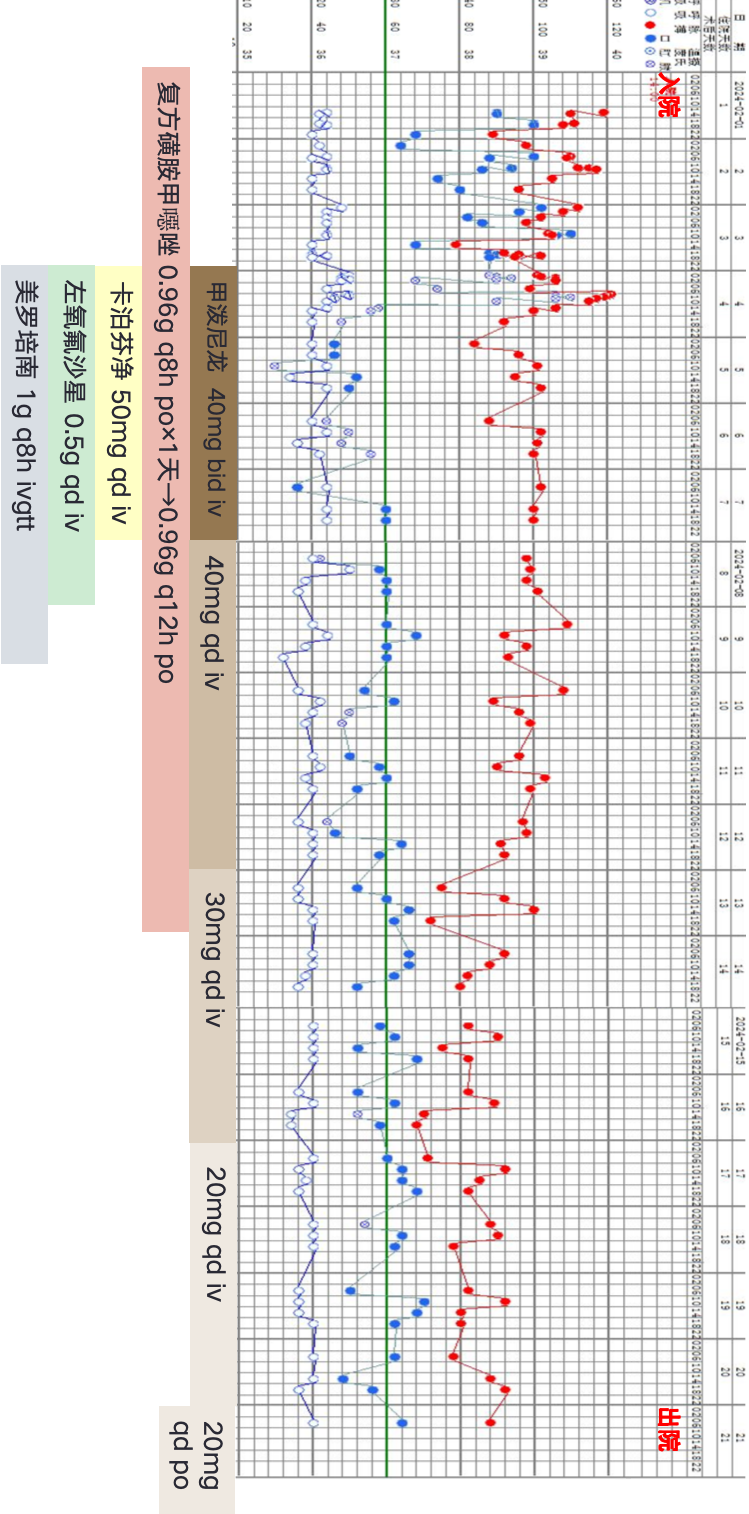
体温变化
炎症标志物变化
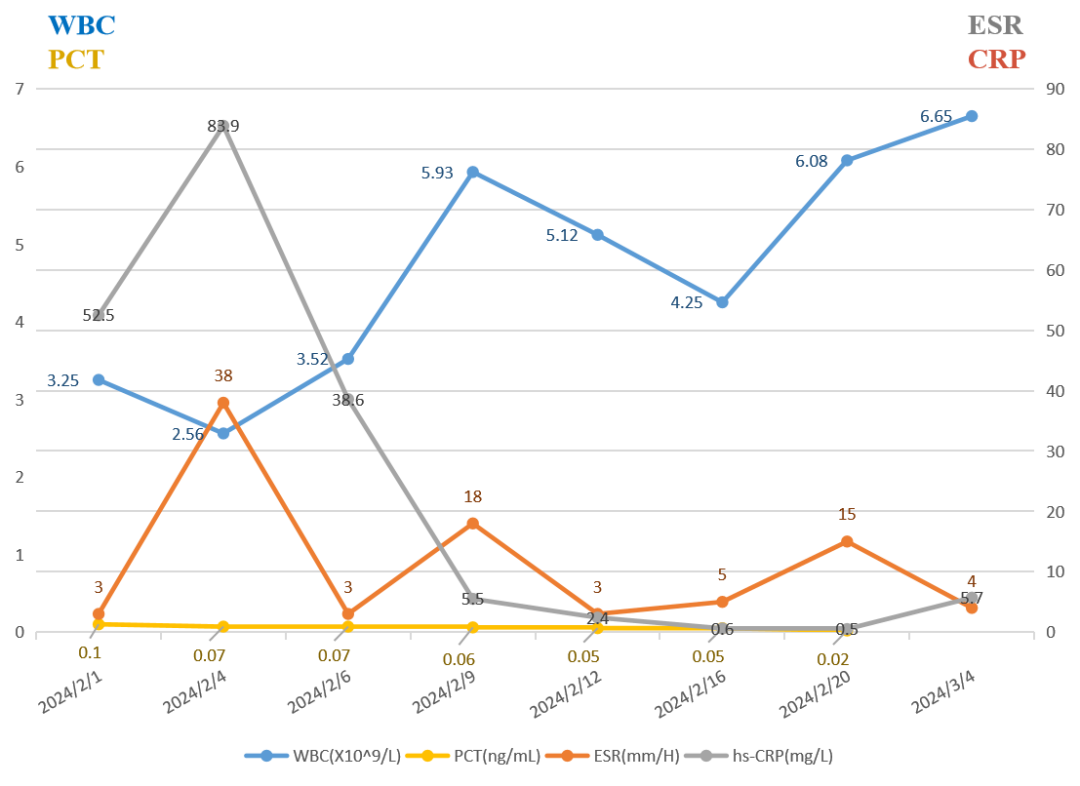
五、最后诊断与诊断依据
最后诊断
1、免疫检查点抑制剂相关肺炎合并肺部感染(细菌、PJ?混合性感染)
2、乙型流感病毒感染
诊断依据
老年男性,食管恶性肿瘤基础,化疗及免疫治疗后,本次症状表现为急性起病的发热、咳嗽咳痰、胸闷气促,血白细胞降低、CRP升高,乙流核酸阳性,痰肺孢子菌DNA阳性,肺部CT表现为左肺为主的双肺斑片状模糊影,初步考虑感染可能大(PJ可能),予SMZ及抗乙流治疗后效果不佳,患者低氧进一步加重,炎症指标升高,胸部CT提示肺炎短期进展明显,结合患者既往抗PD-L1治疗史及痰NGS(流感嗜血杆菌/HHV-7)、血NGS(极少量耶氏肺孢子菌)结果,考虑免疫相关性肺炎,合并细菌、PJ感染不除外,加用糖皮质激素、美罗培南、左氧氟沙星、卡泊芬净治疗后患者炎症指标好转,复查胸部CT见病灶显著吸收。后患者多次送检痰涂片、培养均阴性,痰真菌三项阴性,白细胞不高,炎症指标轻度升高/正常,细菌、PJ等病原体感染证据不足,停用抗菌药物,继续激素治疗,随访血气提示低氧症状持续改善,血炎症指标正常,肺部CT见病灶进一步吸收,综合患者既往用药史、血炎症指标、痰病原学检查结果、激素治疗反应及肺部影像学变化,诊断为免疫检查点抑制剂相关肺炎合并肺部感染(细菌、PJ?混合性感染)。
六、经验与体会
1、近年来,以免疫检查抑点制剂(immune checkpoint inhibitors,ICIs)为代表的免疫疗法在恶性肿瘤的临床治疗方面取得了极大的进展。然而ICIs在介导活化T细胞攻击肿瘤细胞的同时,也可能会对正常组织器官进行攻击,从而引起各种免疫相关不良事件。ICIs引发的肺炎称为免疫检查点抑制剂相关肺炎(immune checkpoint inhibitor-related pneumonitis,CIP),总体发生率为5%,引发速度不一,中位时间为2.8个月,有时在治疗超过1年后才发生。CIP的发生机制尚不明确,形成假说包括总体和/或靶向T细胞针对良恶性组织共有的自身抗原的活性增高,炎症细胞因子水平增加,已有的自身抗体和补体介导炎症的增加等。
2、CIP的症状一般表现为呼吸困难、咳嗽、发热,大多症状较轻(约73%),有时会伴随其他免疫相关不良反应,如结肠炎、皮炎或甲状腺炎。若正在接受ICI治疗的患者新发咳嗽、呼吸急促、劳力性呼吸困难或此类症状加重,应考虑ICI相关肺炎。CIP的影像学表现多样,胸部CT可表现为双肺散在或弥漫性磨玻璃影、斑片状实变影、小叶间隔可增厚、网格状影等。综上,CIP的临床表现缺乏特异性且尚无特异性血清学标志物,应结合病史、临床症状、实验室检查及影像学等综合分析,通常是一种排除性诊断,应排除感染、肿瘤进展、放射性肺炎等。本例患者既往抗PD-L1抗体用药史,以急性发热、咳嗽、胸闷气促为主要表现,血白细胞不高,炎症标志物升高,乙流核酸及痰肺孢子菌DNA阳性,胸部CT示双肺散在片状模糊影,玛巴洛沙韦及SMZ治疗效果不佳,肺部病灶短期明显进展,结合痰NGS提示流感嗜血杆菌,予糖皮质激素及抗菌药物治疗肺部病灶吸收明显,后痰病原学检测持续阴性,停用抗菌药物后激素治疗下肺部病灶进一步吸收,故考虑CIP诊断明确。
3、对于无症状的CIP,通常停药2-4周并密切随访,如果出现症状或影像学进展,可用糖皮质激素治疗;对于症状明显的患者应暂停ICIs,使用糖皮质激素治疗并密切随访。大多数患者在接受糖皮质激素治疗后恢复良好。本例患者肺炎进展迅速,低氧明显,予糖皮质激素治疗后效果佳,随访胸部CT提示肺内病灶持续好转吸收。然而需要注意,由于继发感染、肿瘤进展或免疫抑制剂治疗无效,部分患者的预后仍然很差,且约1/4的CIP患者会复发。CIP治愈后,大多数患者在重启免疫治疗后没有复发,但多见于轻症患者。对于症状较重、病灶累及所有肺叶或50%肺实质、需住院治疗的患者,建议永久停止ICIs治疗。
参考文献
[1] Lin Mei-Xi,Zang Dan,Liu Chen-Guang et al. Immune checkpoint inhibitor-related pneumonitis: research advances in prediction and management.[J] .Front Immunol, 2024, 15: 1266850.
[2] Berner Fiamma,Flatz Lukas,Autoimmunity in immune checkpoint inhibitor-induced immune-related adverse events: A focus on autoimmune skin toxicity and pneumonitis.[J] .Immunol Rev, 2023, 318: 37-50.
[3] Owen C N,Bai X,Quah T et al. Delayed immune-related adverse events with anti-PD-1-based immunotherapy in melanoma.[J] .Ann Oncol, 2021, 32: 917-925.
[4] Naidoo Jarushka,Wang Xuan,Woo Kaitlin M et al. Pneumonitis in Patients Treated With Anti-Programmed Death-1/Programmed Death Ligand 1 Therapy.[J] .J Clin Oncol, 2017, 35: 709-717.
作者:苑菲菲 金文婷 马玉燕;审阅:胡必杰 潘珏
本文转载自订阅号「SIFIC感染视界」
原链接戳:探案丨似是而非,肺内病灶究竟缘何而起?
* 文章仅供医疗卫生相关从业者阅读参考
本文完
责编:Jerry


