自2022年初以来,新一轮由新冠病毒Omicron毒株引起的疫情在全国扩散。 截至2022年5月25日24时,我国新冠肺炎累计确诊病例223735例,25日新增本土确诊病例130例,本土无症状感染者415例[1] ,疫情防控态势依旧严峻,防控措施不容放松。 战疫两年有余,我们有了更多的「武器」吗?免疫功能低下、有基础疾病等特殊人群该如何应对?
在本期的【新冠防控大咖谈】上,深圳市第三人民医院院长、首届深圳市疫情防控公共卫生专家组组长卢洪洲教授带来了《新冠病毒病的科学防控》,聚焦目前的疫情情况和后续防控措施。
新冠病毒介绍与流行病特征
与既往流行病毒相比,SARS-CoV-2的传染性更强,R0值约为2.5(1.8~3.6)[2],德尔塔变异株的再生数R0为5.08[3],远高于原始毒株,而奥密克戎变异株R0更是德尔塔的2.5倍[4]。但奥密克戎感染后临床症状轻于德尔塔,下呼吸道受累较少,嗅觉、味觉丧失比例较低[5]。
此外,感染奥密克戎后的重症比例更低[6] ,住院风险和死亡风险大大降低,这与多个因素有关,首先奥密克戎变异株的毒性更低;部分患者可能已感染过其他毒株,产生交叉保护;最重要的是疫苗覆盖率,接种疫苗可以有效降低重症率和死亡风险[7] 。
中和抗体用于COVID-19的治疗
奥密克戎感染后多数为轻症,在7-10天后,92%的病人可康复。但如果为高危人群,如老年患者、肿瘤患者等可能发展为重症,对于这部分病人,应当早期抗病毒治疗,防止病情进展。我国最新发布的《新型冠状病毒肺炎诊疗方案(试行第九版)》中将安巴韦单抗/罗米司韦单抗注射液推荐用于轻型和普通型且伴有具有进展为重症高风险因素的成人和青少年(12-17岁,体重≥40kg),而Paxlovid推荐用于发病5天内的轻型和普通型且伴有具有进展为重症高风险因素的成人[8]。
单克隆抗体(mAb)是由单个B细胞克隆产生的抗体,具有单特异性,与同一表位相结合,属于被动免疫[9],是一类新型的抗病毒干预措施。单克隆抗体对抗病毒感染的作用机制包括中和作用、促进感染细胞调亡和免疫调理促进病毒清除作用[10]。而作为单克隆中和抗体联合药物的安巴韦单抗/罗米司韦单抗效果更优于单个抗体。
在III期临床试验ACTIV-2[11]中,与安慰剂相比,安巴韦单抗/罗米司韦单抗显著降低具有发展为重症风险的成年轻中症新冠患者住院或死亡风险80%(P<0.00001),治疗组28天治疗期内无死亡病例,而安慰剂组有9例死亡。中期分析显示,在新冠病程后期(即症状发生6-10天)开始治疗的患者中,安巴韦单抗/罗米司韦单抗降低住院或死亡风险与早期应用效果一致。
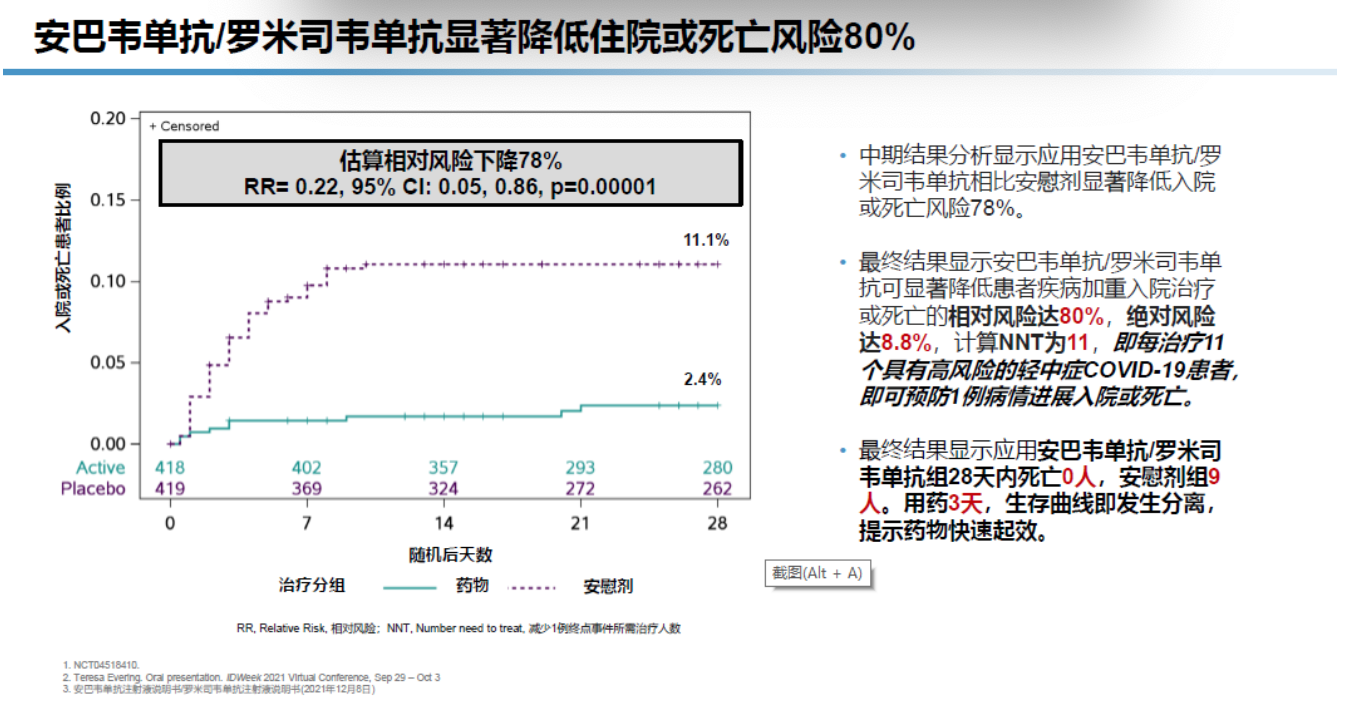 ACTIV-2研究
ACTIV-2研究
除了强效降低重症/死亡风险的临床获益外,安巴韦单抗/罗米司韦单抗还可以广谱抗突变株。体外实验提示,对于目前所有包括奥密克戎BA.2在内的VOC变异株,安巴韦单抗/罗米司韦单抗均保持治疗活性[12]。与PAXLOVID相比,安巴韦单抗/罗米司韦单抗在肝肾功能不全的患者中亦可应用,无需调整剂量,且安巴韦单抗/罗米司韦单抗无药物相互作用。安巴韦单抗/罗米司韦单抗可用于首发症状10天以内的新冠患者,而PAXLOVID则适用于首发症状5天以内的患者。此外,安巴韦单抗/罗米司韦单抗半衰期为46-76天,是普通抗体2-4倍,单次注射后血药浓度可提供长期免疫保护[13]。
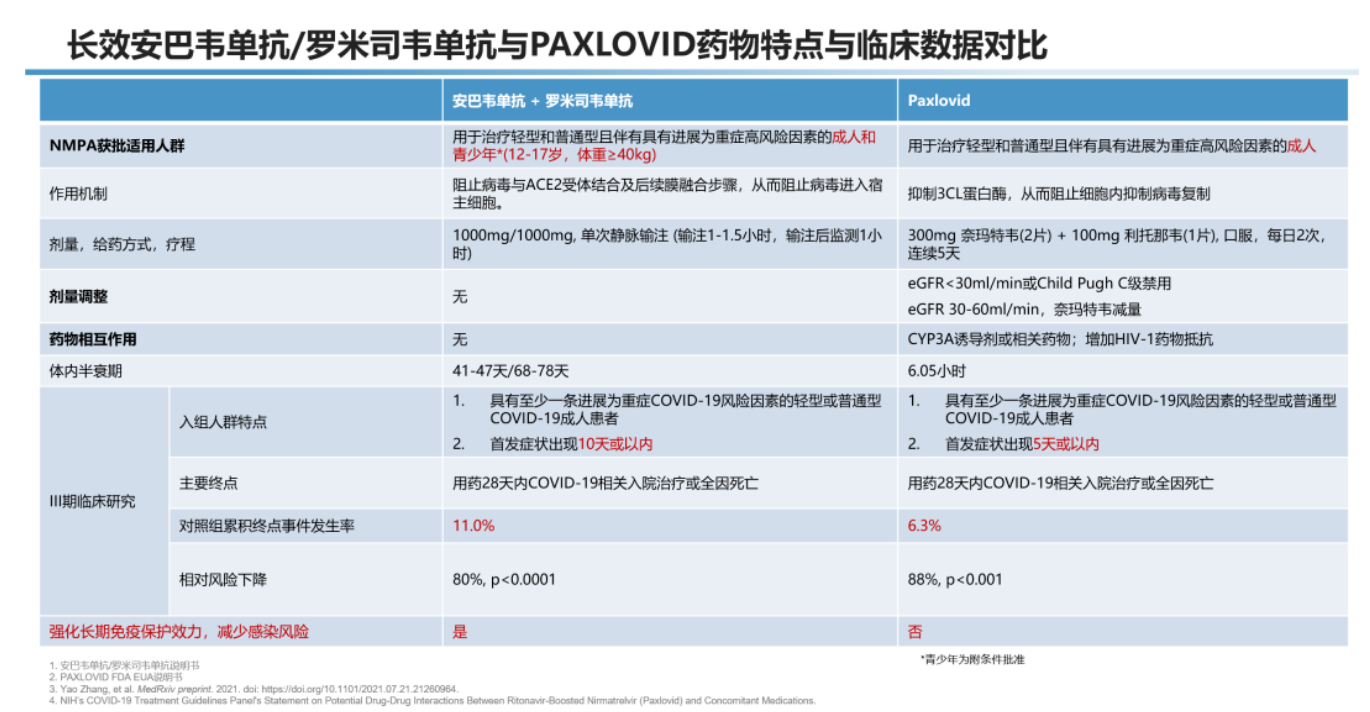

安巴韦单抗/罗米司韦单抗与PAXLOVID对比
中和抗体用于特殊人群COVID-19预防
美国国立卫生院对中重度免疫功能低下且可能对COVID-19疫苗无有效免疫应答和对疫苗及成分有严重不良反应导致无法接种的患者推荐使用长效中和抗体进行暴露前预防[14]。例如,多数肿瘤患者对疫苗反应差,接种疫苗后仍容易发生突破性感染并进展为重症或死亡[15]。卢洪洲教授指出,对于这类病人同样可以注射单抗或单抗组合药物进行暴露前预防,可以有效预防新冠重症和死亡。
前文提到安巴韦单抗和罗米司韦单抗Fc区域经过YTE改造后,半衰期显著延长,分别为44.6-48.6天/72.2-83.0天。研究显示,注射6个月时,体内针对德尔塔毒株的中和抗体滴度仍显著高于接种灭活疫苗加强针后2周时的血浆中和抗体滴度[13] ,为患者提供了长期免疫保护。在全球获批的中和抗体药物中,安巴韦单抗/罗米司韦单抗的综合表现同样优秀。
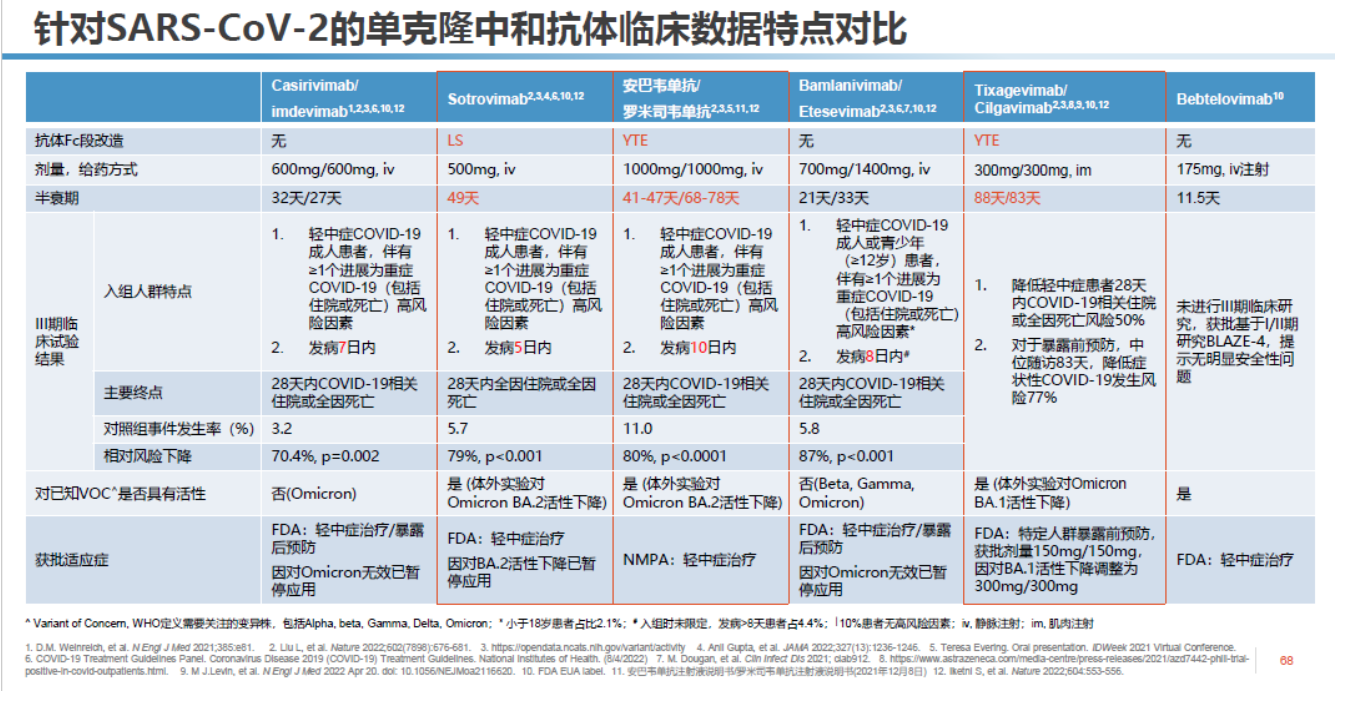
中和抗体临床数据对比
最后,卢洪洲教授总结道,单克隆中和抗体可用于COVID-19治疗和预防,并给人群提供长期免疫保护,不管在暴露前预防、暴露后预防还是治疗方面,均有其价值。
参考文献
[1]http://www.nhc.gov.cn/xcs/yqfkdt/202205/5c8da9563f044166b2952fadd1813c60.shtml
[2] Petersen E, Koopmans M, Go U, etal. Comparing SARS-CoV-2 with SARS-CoV and influenza pandemics[J]. Lancet Infect Dis. 2020;20(9):e238-e244.
[3] Liu Y, Rocklöv J. The reproductive number of the Delta variant of SARS-CoV-2 is far higher compared to the ancestral SARS-CoV-2 virus[J]. J Travel Med. 2021;28(7):taab124.
[4] Liu Y, Rocklöv J. The effective reproduction number for the omicron SARS-CoV-2 variant of concern is several times higher than Delta[J]. J Travel Med. 2022:taac037.
[5] Menni C, Valdes AM, Polidori L, et al. Symptom prevalence, duration, and risk of hospital admission in individuals infected with SARS-CoV-2 during periods of omicron and delta variant dominance: a prospective observational study from the ZOE COVID Study[]J. Lancet. 2022 ;399(10335):1618-1624.
[6] Madhi SA, Kwatra G, Myers JE, et al. Population Immunity and Covid-19 Severity with Omicron Variant in South Africa[J]. N Engl J Med. 2022;386(14):1314-1326.
[7] Andrews N, Stowe J, Kirsebom F,etal. Covid-19 Vaccine Effectiveness against the Omicron (B.1.1.529) Variant[J]. N Engl J Med. 2022;386(16):1532-1546.
[8]中国国家卫生健康委员会. 新型冠状病毒肺炎诊疗方案(试行第九版)[J]. 国际流行病学传染病学杂志,2022,49(2):73-80.
[9] Breedveld FC. Therapeutic monoclonal antibodies[J]. Lancet. 2000;355(9205):735-40.
[10] Taylor PC, Adams AC, Hufford MM,etal. Neutralizing monoclonal antibodies for treatment of COVID-19[J]. Nat Rev Immunol. 2021 ;21(6):382-393.
[11] Teresa Evering. Oral presentation. IDWeek 2021 Virtual Conference, Sep 29 – Oct 3
[12] https://www.briibio.com/news-detail.php?id=1470#news
[13] Yao Zhang, et al. MedRxiv preprint . 2021. doi : https://doi.org/10.1101/2021.07.21.21260964.
[14] NIH’s COVID-19 Treatment Guidelines Panel's Statement on Therapies for High-Risk, Non-hospitalized Patients With Mild to Moderate COVID-19.
[15] Shapiro LC, Thakkar A, Campbell ST, etal. Efficacy of booster doses in augmenting waning immune responses to COVID-19 vaccine in patients with cancer[J]. Cancer Cell. 2022 ;40(1):3-5.
专家介绍

卢洪洲教授长期从事传染病学的临床、科研和教学工作。在SARS疫情期间,卢洪洲教授奔赴多地进行疫情防控工作;诊断H7N9首个病例,因在H7N9疫情防控上的重要贡献,卢教授荣获国家科学技术进步奖特等奖。
2021年,美国斯坦福大学发布全球前2%顶尖科学家排行榜,卢洪洲教授入选终身科学影响力排行榜。


